
I. PHẦN CHUNG: (8,0đ) Dành cho tất cả các thí sinh
1. (2,0đ) Hoàn thành các phương trình hóa học sau dưới dạng phân tử và phương trình ion rút gọn:
a) KOH + HCl →
b) Ca(NO3)2 + Na2CO3 →
2. (2,0đ) Bằng phương pháp hóa học hãy phân biệt các dung dịch bị mất nhãn sau: Ba(NO3)2, Na3PO4, KCl, NaNO3
3. (2,0đ) Viết các phương trình phản ứng hóa học thực hiện chuỗi phản ứng sau: 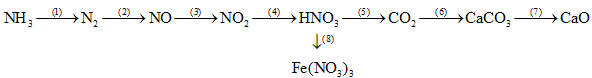
4. (2,0đ) Cho 1,2 gam hỗn hợp X gồm Mg và MgO tác dụng hoàn toàn với 39,4 gam dung dịch HNO3 loãng thì thu được 0,448 lít khí NO (đktc) (sản phẩm khử duy nhất) và dung dịch A.
a) Tính thành phần phần trăm theo khối lượng mỗi chất có trong 1,2 gam hỗn hợp X.
A. 70% và 30%. B. 60% và 40%.
C. 50% và 50%. D. 20% và 80%.
b) Tính nồng độ phần trăm của muối có trong dung dịch A.
A. 14,54% B. 16,54%
C. 14,45% D. 15,54%
II. PHẦN TỰ CHỌN: (2,0đ) Thí sinh chỉ được chọn một trong hai câu: 5.A hoặc 5.B để làm bài
5.A: (2,0đ) Theo chương trình chuẩn
Đốt cháy hoàn toàn 1,48 gam một hợp chất hữu cơ sau phản ứng thu được 3,52 gam CO2 và 1,8 gam H2O
Advertisements (Quảng cáo)
a) Tìm công thức đơn giản nhất của hợp chất hữu cơ.
A. C4H10O. B. C2H5O.
C. CH4O. D. C2H4O.
b) Tìm công thức phân tử của hợp chất hữu cơ biết khi hóa hơi 7,4 gam hợp chất hữu cơ có thể tích đúng bằng thể tích của 3,2 gam oxi (đo ở cùng điều kiện nhiệt độ, áp suất)
A. C2H6O. B. C2H4O.
C. C4H10O. D. C3H6O2.
5.B: (2,0đ) Theo chương trình nâng cao
Cho dung dịch X có chứa axit HCOOH 0,1M có hằng số phân li là Ka = 1,6.10-4 (Bỏ qua sự điện li của H2O)
a) Tính pH của dung dịch X.
A. 2,4. B. 2,2.
C. 2,6. D. 2,3.
Advertisements (Quảng cáo)
b) Tính độ điện li của HCOOH.
A. 3,29%. B. 3,92%.
C. 2,93%. D. 2,39%.
c) Khi cho 5,85 gam NaCl vào dung dịch X thì độ điện li của HCOOH như thế nào? Giải thích?
A. Tăng.
B. Giảm.
C. Tăng sau đó giảm dần.
D. Không đổi.

1. a) Phương trình phân tử: KOH + HCl → KCl + H2O
Phương trình ion rút gọn: OH– + H+ → H2O
b) Phương trình phân tử: Ca(NO3)2 + Na2CO3 → CaCO3↓ + 2NaNO3
Phương trình ion rút gọn: Ca2+ + CO32- → CaCO3↓
2.
|
Chất thử Thuốc thử |
Ba(NO3)2 |
Na3PO4 |
KCl |
NaNO3 |
|
AgNO3 |
Không hiện tượng |
↓ vàng |
↓ trắng |
Không hiện tượng |
|
Na2SO4 |
↓ trắng |
– |
– |
Không hiện tượng |
PTHH:
Na3PO4 + 3AgNO3 → Ag3PO4↓ vàng+ 3NaNO3
KCl + AgNO3 → KNO3 + AgCl↓ trắng
Ba(NO3)2 + Na2SO4 → 2NaNO3 + BaSO4↓ trắng
3.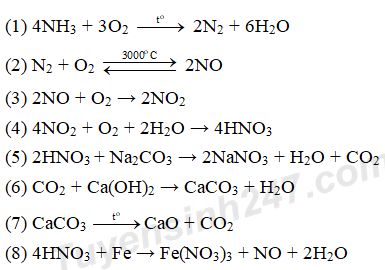
4. a) Đáp án B
b) Đáp án D
5.A: a) Đáp án A
b) Đáp án C
5.B: a) Đáp án A
b) Đáp án B
c) Đáp án D





