Các em và thầy cô tham khảo Đề cương ôn tập kiểm tra, thi học kì 1 lớp 9 môn Hóa học gồm phần lý thuyết và các dạng bài tập.
Các em sẽ quan tâm:Ôn lại toàn bộ lý thuyết và bài tập trong SGK Hóa lớp 9:
SỞ GIÁO GD- ĐT BÀ RỊA VŨNG TÀU
HỘI ĐỒNG BỘ MÔN HÓA HỌC
ĐỀ CƯƠNG ÔN TẬP HỌC KỲ I
MÔN: HÓA HỌC 9
I. Lý thuyết :
- Tính chất hóa học của : oxit, axit, bazơ, muối, kim loại, phi kim
- Tính chất hóa học của axit sunfuaric đặc, nhôm, clo.
- Phân bón hóa học.
- Các biện pháp chống ăn mòn kim loại
- Dãy hoạt động hóa học của kim loại và ý nghĩa của nó.
- Tính chất vật lý của CaO, SO2, H2SO4, NaOH, Al,Fe, Cl2.
- Điều chế: SO2 , CaO, H2SO4, NaOH, Al, Cl2
- Ứng dụng của CaO, NaCl, Al, Fe ( gang- thép)
- Điều kiện để phản ứng xảy ra trong dung dịch.
- Lưu ý học lại tính tan và xem các hiện tương xảy ra trong các thí ngiệm trong sgk, màu sắc của các chất, các dung dịch dã biết.
II. Các dạng bài tập:
- Viết các pthh minh họa cho tính chất hóa học, ứng dụng của các chất, pthh điều chế các chất.
- Dựa vào tính chất hóa học, vật lý giải thích các ứng dụng, các hiện tượng thường gặp.
- Viết pthh hoàn thành dãy chuyển hóa, thể hiện mối quan hệ giữa các loại hợp chất vô cơ.
- Phân biệt, nhận biết các chất bằng phương pháp vật lý, hóa học.
- Các bài tập định lượng : áp dụng tính theo pthh, định luật bảo toàn khối lượng , tính nồng độ dung dịch, tính khối lượng kết tủa, tính thể tích chất khí (đktc), tính thành phần trong hỗn hợp ban đầu hoặc hổn hợp sản phẩm, xác định tên nguyên tố. ..
III. Phần mở rộng.
- Áp dụng các kiến thức mở rộng trong phần em có biết.
- Phản ứng giữa oxit axit với dung baz ơ.
- Phản ứng giữa kim loại với axit sunfuaric đặc nóng.
- Phản ứng giữa Al, Zn với dung dịch baz ơ.
Đề cương cụ thể và một số bài tập tham khảo kiểm tra, thi học kì 1 môn Hóa 9
- OXIT
a) Định nghĩa: Oxit là hợp chất gồm 2 nguyên tố, trong đó có một nguyên tố là oxi.
Vd: CaO, SO2, CO, Na2O, Fe3O4, P2O5, …
b) Tính chất hóa học: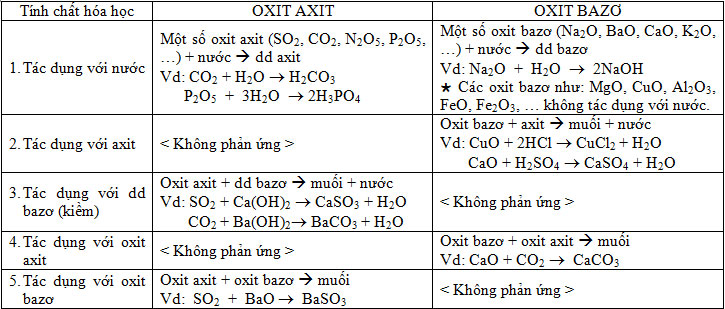
- AXIT
a) Định nghĩa: Axit là hợp chất mà phân tử gồm có một hay nhiều nguyên tử H liên kết với gốc axit. Các nguyên tử H này có thể thay thế bằng các ng/tử kim loại.
Vd: HCl, HNO3, H2SO4, H3PO4, …
b) Tính chất hóa học:
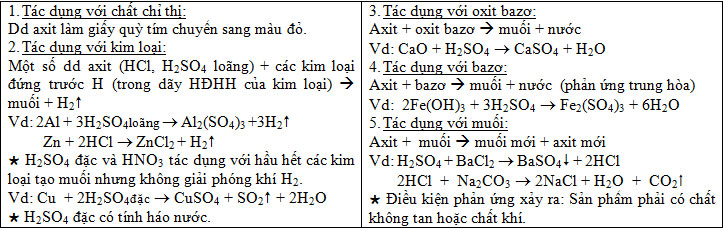
Sản xuất axit sunfuric: Gồm các công đoạn sau:
(1) S + O2 t0,V2O5 → SO2
(2) 2SO2 + O2 → 2SO3
(3) SO3 + H2O → H2SO4
- BAZƠ
a) Định nghĩa: Bazơ là hợp chất mà phân tử gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (OH).
Vd: KOH, NaOH, Ba(OH)2, Al(OH)3, …
b) Tính chất hóa học:
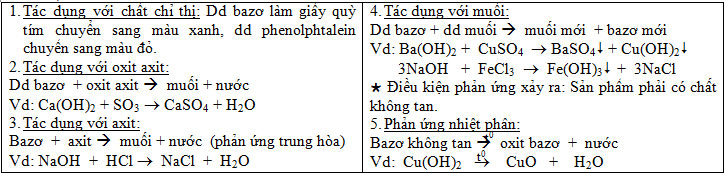
Sản xuất natri hiđroxit:
2NaCl + H2O điện phân dd, có màng ngăn → 2NaOH + Cl2 + H2
c) Thang pH: Dùng để biểu thị độ axit hoặc độ bazơ của một dung dịch:
pH = 7: trung tính ; pH < 7: tính axit ; pH > 7: tính bazơ
- MUỐI
a) Định nghĩa: Muối là hợp chất mà phân tử có một hay nhiều nguyên tử kim loại liên kết với một hay nhiều gốc axit. Vd: NaCl, MgSO4, Fe(NO3)2, BaCO3, …
b) Tính chất hóa học:
c) Phản ứng trao đổi:
- Định nghĩa: Là phản ứng hóa học, trong đó hai hợp chất tham gia phản ứng trao đổi với nhau những thành phần cấu tạo của chúng để tạo ra những hợp chất mới.
Vd: BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Na2CO3 + 2HCl → 2NaCl↓ + H2O + CO2↑
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
NaCl + AgNO3 → AgCl↓ + NaNO3
- Điều kiện để phản ứng trao đổi xảy ra: Phản ứng trao đổi trong dung dịch của các chất chỉ xảy ra nếu sản phẩm tạo thành có chất không tan hoặc chất khí.
Lưu ý: Phản ứng trung hòa cũng là phản ứng trao đổi và luôn xảy ra.
Vd: NaOH + HCl → NaCl + H2O
III – KIM LOẠI:
- TÍNH CHẤT CHUNG CỦA KIM LOẠI
a) Tính chất vật lý:
- Có tính dẻo, dễ dát mỏng và dễ kéo sợi.
- Dẫn điện và dẫn nhiệt tốt. (Ag là kim loại dẫn điện và dẫn nhiệt tốt nhất, tiếp theo là Cu, Al, Fe, …)
- Có ánh kim.
b) Tính chất hóa học:
SO SÁNH TÍNH CHẤT CỦA NHÔM VÀ SẮT:
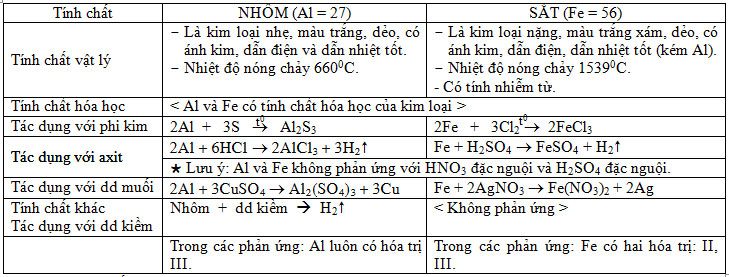
Sản xuất nhôm:
- Nguyên liệu: quặng boxit (thành phần chủ yếu là Al2O3), than cốc, khơng khí.
- Phương pháp: điện phân nóng chảy.
2Al2O3 Điện ph nóng chảy, criolit→ 4Al + 3O2
- DÃY HOẠT ĐỘNG HÓA HỌC CỦA KIM LOẠI
Theo chiều giảm dần độ hoạt động của kim loại:
K, Na, Ca, Mg, Al, Zn, Fe, Pb, (H), Cu, Ag, Au
Ý nghĩa dy hoạt động hóa học của kim loại:
- Mức độ họat động hóa học của kim loại giảm dần từ trái qua phải.
- Kim loại đứng trước Mg tác dụng với nước ở điều kiện thường à kiềm và khí hiđro.
- Kim loại đứng trước H phản ứng với một số dd axit (HCl, H2SO4 loãng, …) à khí H2.
- Kim loại đứng trước (trừ Na, K…) đẩy kim loại đứng sau ra khỏi dung dịch muối.
- HỢP CHẤT SẮT: GANG, THÉP
a) Hợp kim: Là chất rắn thu được sau khi làm nguội hỗn hợp nóng chảy của nhiều kim loại khác nhau hoặc hỗn hợp kim loại và phi kim.
b) Thành phần, tính chất và sản xuất gang, thép:
| Hợp kim | GANG | THÉP |
| Thành phần | Hàm lượng cacbon 2 – 5%; 1 – 3% các nguyên tố P, Si, S, Mn; còn lại là Fe. | Hàm lượng cacbon dưới 2%; dưới 0,8% các nguyên tố P, S, Mn; còn lại là Fe. |
| Tính chất | Giòn, không rèn, không dát mỏng được. | Đàn hồi, dẻo (rèn, dát mỏng, kéo sợi được), cứng. |
| Sản xuất | – Trong lò cao.
– Nguyên tắc: CO khử các oxit sắt ở t0 cao.3CO + Fe2O3 →3CO2 + 2Fe |
– Trong lò luyện thép.
– Nguyên tắc: Oxi hóa các nguyên tố C, Mn, Si, S, P, … có trong gang. FeO + C → Fe + CO |
IV – PHI KIM:
- TÍNH CHẤT CHUNG CỦA PHI KIM
a) Tính chất vật lý:
- Ở điều kiện thường, phi kim tồn tại ở cả 3 trạng thái: rắn (S, P, …) ; lỏng (Br2) ; khí (Cl2, O2, N2, H2, …).
- Phần lớn các nguyên tố phi kim không có ánh kim, dẫn điện, dẫn nhiệt kém; Nhiệt độ nóng chảy thấp.
- Một số phi kim độc như: Cl2, Br2, I2.
b) Tính chất hóa học:
| 1. Tác dụng với kim loại: Nhiều phi kim + kim loại → muối:
Vd: 2Na + Cl2 t0 → 2NaCl Oxi + kim loại → oxit: Vd: 2Cu + O2 → 2CuO 2. Tác dụng với hiđro: Oxi + khí hiđro → hơi nước 2H2 + O2 → 2H2O Clo + khí hiđro → khí hiđro clorua H2 + Cl2 → 2HCl Nhiều phi kim khác (C, S, Br2, …) phản ứng với khí hiđro tạo thành hợp chất khí. |
3. Tác dụng với oxi:Nhiều phi kim + khí oxi → oxit axit
Vd: S + O2 t0→ SO2 4P + 5O2 t0→ 2P2O5 4. Mức độ hoạt động hóa học của phi kim: – Mức độ hoạt động hóa học mạnh hay yếu của phi kim thường được xét căn cứ vào khả năng và mức độ phản ứng của phi kim đó với kim loại và hiđro. – Flo, oxi, clo là những phi kim hoạt động mạnh (flo là phi kim hoạt động mạnh nhất). – Lưu huỳnh, photpho, cacbon, silic là những phi kim hoạt động yếu hơn. |
- SO SÁNH TÍNH CHẤT CỦA CLO VÀ CACBON
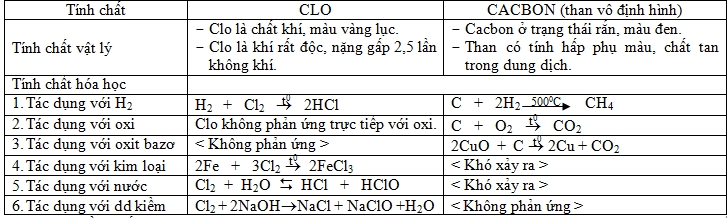
Điều chế clo:
- Trong phòng thí nghiệm: MnO2 + HClđặc → MnCl2 + Cl2 + H2O
- Trong công nghiệp: 2NaCl + H2O Điện phân, có màng ngăn → 2NaOH + Cl2 + H2
- CÁC OXIT CỦA CACBON
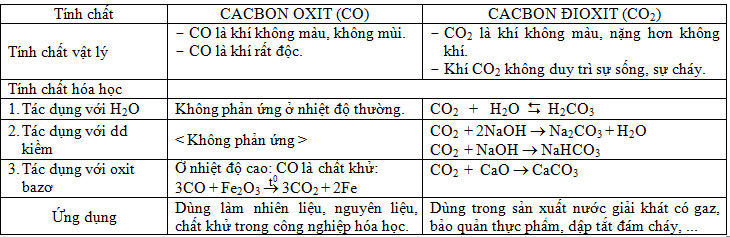
TÍNH TAN TRONG NƯỚC CỦA MỘT SỐ DUNG DỊCH BAZƠ, MUỐI:
| Bazơ tan | KOH, NaOH, Ba(OH)2, Ca(OH)2 ít tan. |
| Bazơ không tan | Mg(OH)2, Fe(OH)2, Fe(OH)3, Zn(OH)2, Cu(OH)2, Al(OH)3, Pb(OH)2 |
| Muối Sunfat (=SO4) | Hầu hết tan (trừ BaSO4, PbSO4 không tan). |
| Muối Sunfit (=SO3) | Hầu hết không tan (trừ K2SO3 , Na2SO3 tan). |
| Muối Nitrat (-NO3) | Tất cả đều tan. |
| Muối Photphat (≡PO4) | Hầu hết không tan (trừ K3PO4 , Na3PO4 tan ). |
| Muối Cacbonat (=CO3) | Hầu hết không tan (trừ K2CO3 , Na2CO3 tan). |
| Muối Clorua (-Cl ) | Hầu hết đều tan (trừ AgCl không tan). |
HÓA TRỊ CỦA MỘT SỐ NGUYÊN TỐ VÀ NHÓM NGUYÊN TỬ:
| Hóa trị (I) | Hóa trị (II) | Hóa trị (III) | |
| Kim loại | Na, K, Ag | Ca , Ba , Mg , Zn, Fe, Pb, Cu, Hg | Al, Fe |
| Nhóm nguyên tử | -NO3 ; (OH) (I) | =CO3 ; =SO3 ; =SO4 | PO4 |
| Phi kim | Cl , H , F | O |
Các phi kim khác: S (IV,VI ) ; C (IV) ; N (V) ; P (V).
PHẦN B – CÁC DẠNG BÀI TẬP:
Dạng 1: XÉT ĐIỀU KIỆN PHẢN ỨNG – VIẾT PHƯƠNG TRÌNH HÓA HỌC.
Advertisements (Quảng cáo)
Bài 1: Viết các PTHH thực hiện các chuỗi biến hóa sau, ghi rõ điều kiện phản ứng (nếu có):
Bài 2: Viết các phương trình hoá học biễu diễn các chuyển hoá sau: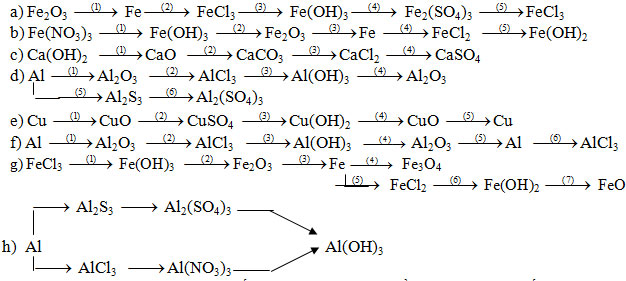
Bài 3: Nêu hiện tượng quan sát được và viết PTHH xảy ra, ghi rõ điều kiện phản ứng (nếu có):
- Cho mẫu kẽm vào ống nghiệm chứa dd HCl(dư)
- Cho mẫu nhôm vào ống nghiệm chứa H2SO4 đặc, nguội.
- Cho dây nhôm vào dd NaOH đặc.
- Cho từ từ dd BaCl2 vào ống nghiệm chứa dd H2SO4.
- Cho từ từ dd BaCl2 vào ống nghiệm chứa dd Na2CO3.
- Cho từ từ dd HCl vào ống nghiệm chưá dd NaOH có để sẵn 1 mẫu giấy quỳ tím.
- Cho đinh sắt vào ống nghiệm chứa dd CuSO4.
- Cho dd NaOH từ từ vào ống nghiệm chứa dd CuSO4. sau đó lọc lấy chất kết tủa rồi đun nhẹ.
- Cho từ từ dd AgNO3 vào ống nghiệm chứa dd NaCl.
- Cho lá đồng vào ống nghiệm chứa dd HCl.
- Đốt nóng đỏ một đoạn dây sắt cho vào bình chứa khí oxi.
- Cho dây bạc vào ống nghiệm chứa dd CuSO4.
- Cho Na(r) vào cốc nước có pha phenolphtalein.
- Rắc bột Al lên ngọn lửa đèn cồn.
- Đun nóng ống nghiệm chứa Cu(OH)2.
Bài 4: Cho các chất sau: CuO, Al, MgO, Fe(OH)2, Fe2O3. Chất nào ở trên tác dụng với dd HCl để:
a) Sinh ra chất khí nhẹ hơn không khí và cháy được trong không khí.
b) Tạo thành dd có màu xanh lam.
c) Tạo thành dd có màu vàng nâu.
d) Tạo thành dd không màu.
Viết các PTHH cho các phản ứng trên.
Bài 5: Cho các chất: Na2CO3, BaCl2, BaCO3, Cu(OH)2, Fe, ZnO. Chất nào ở trên phản ứng với dd H2SO4 loãng để tạo thành:
a) Chất kết tủa màu trắng.
b) Khí nhẹ hơn không khí và cháy được trong không khí.
c) Khí nặng hơn không khí và không duy trì sự cháy.
d) Chất kết tủa màu trắng đồng thời có chất khí nặng hơn không khí và không duy trì sự cháy.
e) Dd có màu xanh lam.
f) Dd không màu.
Viết các PTHH cho các phản ứng trên.
Dạng 2: NHẬN BIẾT CÁC CHẤT
– Nhận biết các chất rắn bằng cách thử tính tan trong nước, hoặc quan sát màu sắc.
– Nhận biết các dd thường theo thứ tự sau:
+ Các dd muối đồng thường có màu xanh lam.
+ Dùng quỳ tím nhận biết dd axit (quỳ tím hóa đỏ) hoặc dd bazơ (quỳ tím hóa xanh).
+ Các dd Ca(OH)2, Ba(OH)2 nhận biết bằng cách dẫn khí CO2, SO2 qua → tạo kết tủa trắng.
+ Các muối =CO3, =SO3 nhận biết bằng các dd HCl, H2SO4 loãng → có khí thoát ra (CO2, SO2)
+ Các muối =SO4 nhận biết bằng các dd BaCl2, Ba(NO3)2, Ba(OH)2 (hoặc ngược lại) à tạo kết tủa trắng.
+ Các muối –Cl nhận biết bằng muối Ag, như AgNO3, Ag2SO4 (hoặc ngược lại). → tạo kết tủa trắng.
+ Các muối của kim loại đồng nhận biết bằng dd kiềm như NaOH, Ca(OH)2, …→ tạo kết tủa xanh lơ.
– Nhận biết các kim loại, chú ý:
+ Dãy hoạt động hóa học của kim loại.
+ Fe, Al không phản ứng với dd H2SO4 đặc, nguội.
+ Al có phản ứng với dd kiềm tạo khí H2.
Bài 1: Nhận biết các chất theo các yêu cầu sau đây:
- Bằng phương pháp hóa học hãy nhận biết các chất rắn sau:
a) CaO, Na2O, MgO, P2O5. b) CaCO3, CaO, Ca(OH)2.
- Chỉ dùng thêm quỳ tím, hãy nhận biết các dung dịch sau:
a) H2SO4, NaOH, HCl, BaCl2. b) NaCl, Ba(OH)2, NaOH, H2SO4.
- Bằng phương pháp hóa học, hãy nhận biết các dung dịch:
a) CuSO4, AgNO3, NaCl.
b) NaOH, HCl, NaNO3, NaCl.
c) KOH, K2SO4, K2CO3, KNO3.
- Chỉ dùng dd H2SO4 loãng, nhận biết các chất sau:
a) Các chất rắn: Cu(OH)2, Ba(OH)2, Na2CO3
b) Các dd: BaSO4, BaCO3, NaCl, Na2CO
- Hãy nêu phương pháp hóa học để nhận biết các kim loại sau:
a) Al, Zn, Cu. b) Fe, Al, Ag, Mg.
Advertisements (Quảng cáo)
Bài 2: Tinh chế.
- Tinh chế bột sắt từ hỗn hợp bột sắt và bột nhôm bằng phương pháp hóa học.
- Tinh chế vụn đồng từ hỗn hợp vụn các kim loại sau: Cu, Zn, Fe.
- Có dd muối AlCl3 lẫn tạp chất là CuCl2. Nêu phương pháp hóa học làm sạch muối nhôm.
- Dung dịch ZnSO4 có lẫn tạp chất là CuSO4. Nêu phương pháp làm sạch dd ZnSO4.
Dạng 3: ĐIỀU CHẾ.
Bài 1: Từ các chất: Fe, Cu(OH)2, HCl, Na2CO3, hãy viết các PTHH điều chế:
a) Dd FeCl2. b) Dd CuCl2. c) Khí CO2. d) Cu kim loại.
Bài 2: Từ các chất: CaO, Na2CO3 và H2O, viết PTHH điều chế dd NaOH.
Bài 3: Từ những chất: Na2O, BaO, H2O, dd CuSO4, dd FeCl2, viết các PTHH điều chế:
a) Dd NaOH. b) Dd Ba(OH)2. c) BaSO4. d) Cu(OH) e) Fe(OH)2
Dạng 4: BÀI TOÁN TÍNH THEO PHƯƠNG TRÌNH HÓA HỌC.
Bài 1: Cho một khối lượng mạt sắt dư vào 150ml dd HCl. Sau phản ứng thu được 10,08 l khí (đktc).
a) Viết PTHH
b) Tính khối lượng mạt sắt tham gia phản ứng.
c) Tính nồng độ mol của dd HCl đã dùng.
Bài 2: 6,72 l khí CO2 (đktc) tác dụng vừa hết với 600ml dd Ba(OH)2, sản phẩm tạo thành là BaCO3 và nước.
a) Viết PTHH.
b) Tính nồng độ mol của dd Ba(OH) đã dùng.
c) Tính khối lượng kết tủa tạo thành.
Bài 3: Trung hòa dd KOH 2M bằng 250ml HCl 1,5M.
a) Tính thể tích dd KOH cần dùng cho phản ứng.
b) Tính nồng độ mol của dd muối thu được sau phản ứng.
c) Nếu thay dd KOH bằng dd NaOH 10% thì cần phải lấy bao nhiêu gam dd NaOH để trung hòa hết lượng axit trên.
Bài 4: Ngâm 1 lá kẽm trong 32g dd CuSO4 10% cho tới khi kẽm không thể tan được nữa.
a) Viết PTHH. Phản ứng trên thuộc loại phản ứng gì?
b) Tính khối lượng kẽm đã phản ứng.
c) Xác định nồng độ % của dd sau phản ứng.
Bài 5: Trung hòa dd KOH 5,6% (D = 10,45g/ml) bằng 200g dd H2SO4 14,7%.
a) Tính thể tích dd KOH cần dùng.
b) Tính C% của dd muối sau phản ứng.
Bài 6: Cho dd NaOH 2M tác dụng hoàn toàn với 3,36l khí clo (đktc).
a) Tính thể tích dd NaOH tham gia phản ứng.
b) Tính nồng độ các chất sau phản ứng. (Giả thuyết cho thể tích dd thay đổi không đáng kể).
Bài 7: Cho 7,75g natri oxit tác dụng với nước, thu được 250ml dd bazơ.
a) Tính nồng độ mol của dd bazơ thu được.
b) Tính khối lượng dd H2SO4 20% cần dùng để trung hòa hết lượng bazơ nói trên. Từ đó tính thể tích dd H2SO4 đem dùng, biết D(dd H2SO4) = 1,14g/ml.
Bài 8: Hòa tan 21,1g hỗn hợp A gồm Zn và ZnO bằng 200g dd HCl (vừa đủ) thu được dd B và 4,48 l khí H2.
a) Xác định khối lượng mỗi chất có trong hỗn hợp A.
b) Tính C% của dd HCl đã dùng.
c) Tính khối lượng muối có trong dd B.
Bài 9: Cho 21g hỗn hợp bột nhôm và nhôm oxit tác dụng với dd HCl dư làm thoát ra 13,44 l khí (đktc).
a) Tính thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp đầu.
b) Tính thể tích dd HCl 36% (D = 1,18g/ml) để hòa tan vừa đủ hỗn hợp đó.
Bài 10: Cho 15,75g hỗn hợp 2 kim loại Cu và Zn vào dd H2SO4 loãng dư, thu được 33,6l khí (đktc).
a) Tính khối lượng mỗi kim loại trong hỗn hợp đầu.
b) Tính khối lượng dd muối thu được.
Bài 11: Hòa tan hoàn toàn 12,1g hỗn hợp bột CuO và ZnO vào 150ml dd HCl 2M.
a) Tính thành phần phần trăm theo khối lượng mỗi oxit trong hỗn hợp đầu.
b) Tính khối lượng dd H2SO4 20% cần để hòa tan hỗn hợp trên.
Bài 12: Cho 10g hỗn hợp Cu và CuO tác dụng với dd H2SO4 loãng dư. Lọc lấy phần chất rắn không tan cho phản ứng với dd H2SO4 đặc, nóng thu được 1,12 l khí (đktc). Tính thành phần % về khối lượng mỗi chất rắn trong hỗn hợp đầu.
Bài 13: Dẫn từ từ 3,136 l khí CO2 (đktc) vào một dd có hòa tan 12,8g NaOH, sản phẩm là muối Na2CO3.
a) Chất nào đã lấy dư, dư bao nhiêu lít (hoặc gam)?
b) Tính khối lượng muối thu được.
Bài 14: Cho 3,92g bột sắt vào 200ml dd CuSO4 10% (D = 1,12g/ml).
a) Tính khối lượng kim loại mới tạo thành.
b) Tính nồng độ mol của chất có trong dd sau phản ứng. (Giả thuyết cho thể tích dd thay đổi không đáng kể).
Bài 15: Trộn 60ml dd có chứa 4,44g CaCl2 với 140ml dd có chứa 3,4g AgNO3.
a) Cho biết hiện tượng quan sát được và viết PTHH.
b) Tính khối lượng chất rắn sinh ra.
c) Tính CM của chất còn lại trong dd sau phản ứng. Biết thể tích dd thay đổi không đáng kể.
Bài 16: Cho 9,2g một kim loại A phản ứng với khí clo (dư) tạo thành 23,4g muối. Xác định tên kim loại A, biết A có hóa trị I.
Bài 17: Cho 0,6g một kim loại hóa trị II tác dụng với nước tạo ra 0,336 l khí H2 (đktc). Tìm kim loại
Bµi 18 :Cho 10,5g hổn hợp hai kim loại Cu, Zn vào dd H2SO4 loãng dư, người ta thu được 2,24 lit khí (đktc)
a) Viết phương trình hóa học.
b) Tính khối lượng chất rắn còn lại trong dd sau phản ứng.
Bài 19: Ngâm một đinh sắt sạch trong 200 ml dd CuSO4. Sau khi phản ứng kết thúc , lấy đinh sắt ra khỏi dung dịch, rửa nhẹ, làm khô, nhận thấy khối lượng đinh sắt tăng thêm 0,8g.
a) Viết phương trình phản ứng.
b) Xác định nồng độ mol của dd CuSo
Bài 20: Cho 0,83g hổn hợp gồm Al và Fe tác dụng với dd H2SO4 loãng dư, sau phản ứng thu được 0,56 lit khí ( đktc)
a) Viết phương trình phản ứng.
b) Tính thành phần % theo khối lượng của hổn hợp ban đầu.
Bài 21: Cho 10,8g kim loại M hóa trị III tác dụng với khí clo dư thu được 53,4g muối . Xác định kim loại M.
Bài 22: Hòa tan 4,5g hợp kim Al – Mg trong dd H2SO4 loãng dư, thấy có 5,04 lít khí H2 bay ra ( đktc).
a) Viết phương trình phản ứng hóa học xãy ra.
b) Tính thành phần % khối lượng của mỗi kim loại trong hổn hợp ban đầu.
Bài 23: Khi hòa tan 6g hổn hợp kim loại gồm Cu, Fe và Al trong axit HCl dư thì tạo thành 3,024 lít khí H2 (đktc) và còn lại 1,86g kim loại không tan.
a) Viết phương trình phản ứng hóa học xãy ra.
b) Tính thành phần % khối lượng của mỗi kim loại trong hổn hợp ban đầu.
Bài 24: Bằng phương pháp hóa học hãy phân biệt các chất sau đây: HNO3, KOH, NaCl vµ Ca(OH)2
Bài 25 :Dẫn từ từ 1,568 lit khí CO2 (đktc) vào một dung dịch có hòa tan 6,4 g NaOH, sản phầm là muối Na2CO3.
a) Hãy xác định khối lượng muối thu được sau phản ứng.
b) Chất nào đã dư và dư là bao nhiêu gam?
Bài 26 :Cho các chất sau: Na2O, Na, NaOH, Na2SO4, Na2CO3, NaCl.
a) Hãy sắp xếp các chất trên thành một dãy chuyển hóa hóa học.
b) Viết các phương trình phản ứng cho dãy chuyển hóa đó.
D.ĐỀ THAM KHẢO:
1 : (2 điểm) Viết các phương trình hóa học thực hiện chuổi biến hóa sau :
Fe3O4 → Fe → FeCl3 → Fe(NO3)3 → Fe(OH)3
2 : (2 điểm)Viết phương trình hóa học (nếu có) khi cho nhôm tác dụng với:
a/ Dung dịch muối đồng (II) sunfat.
b / Axit sunfuric đặc nguội.
c/ Khí clo.
d/ Kẽm clorua
3 : (3 điểm)
a/ Nêu hiện tượng, viết phương trình hóa học trong thí nghiệm sau đây : Nhúng một lá nhôm vào dung dịch CuSO4 màu xanh lam.
b/ Bằng phương pháp hoá học phân biệt ba chất bột sau: nhôm, sắt, bạc.
4 : (3 điểm)
Cho 20g hỗn hợp hai kim loại Zn và Cu tác dụng vừa đủ với 196g dd axit sunfuric, người ta thu được 4,48 lít khí hidro (ở đktc).
a) Viết PTHH của phản ứng.
b) Tính khối lượng các chất có trong hỗn hợp.
c) Tính nồng độ phần trăm dd axit sunfuric cần dùng.






