
I. PHẦN TRẮC NGHIỆM (6đ):
PHẦN CHUNG DÀNH CHO TẤT CẢ CÁC LỚP
1. Cacbohiđrat nào sau đây thuộc loại đisaccarit?
A. Saccarozơ.
B. Glucozơ.
C. Amilozơ.
D. Xenlulozơ.
2. Trong các phản ứng sau, phản ứng nào không chứng minh được nhóm chức anđehit của glucozơ?
A. Lên men glucozơ bằng xúc tác enzim
B. Oxi hóa glucozơ bằng Cu(OH)2 đun nóng
C. Oxi hoá glucozơ bằng AgNO3/NH3
D. Khử glucozơ bằng H2/Ni, t0
3. Phản ứng nào sau đây có thể chuyển glucozơ, fructozơ thành những sản phẩm giống nhau?
A. Phản ứng với H2/Ni, nhiệt độ.
B. Phản ứng với AgNO3/dd NH3.
C. Phản ứng với Cu(OH)2.
D. Phản ứng với Na.
4. Để phân biệt 3 dung dịch H2NCH2COOH, CH3COOH và C2H5NH2 chỉ cần dùng 1 thuốc thử là
A. Quỳ tím
B. Dung dịch HCl
C. Dung dịch NaOH
D. Natri kim loại
5. Công thức tổng quát của este tạo bởi axit đơn chức no mạch hở và ancol đơn chức no mạch hở có dạng.
A. CnH2nO2 (n ≥ 2)
B. CnH2nO2 (n ≥ 3)
C. CnH2n+2O2 (n ≥ 2)
D. CnH2n-2O2 (n ≥ 4)
6. Có bao nhiêu chất đồng phân có cùng công thức phân tử C4H11N
A. 7 chất B. 8 chất
C. 3 chất D. 4 chất
7. Công thức cấu tạo của glyxin là
A. CH3-CH(NH2)-COOH
B. H2N-CH2-COOH
C. H2N-CH2-CH2-COOH
D. CH2(OH)-CH(OH)-CH2OH
8. Mạng tinh thể kim loại gồm có:
A. nguyên tử kim loại và các electron độc thân.
B. nguyên tử, ion kim loại và các electron tự do.
C. nguyên tử, ion kim loại và các electron độc thân.
D. ion kim loại và các electron độc thân.
9. Chất nào dưới đây không phải là este?
A. CH3COOCH3
B. CH3COOH
C. HCOOCH3
D. HCOOC6H5
1.0: Cho phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra:
A. sự khử Fe2+ và sự khử Cu2+
B. sự oxi hóa Fe và sự khử Cu2+
C. sự khử Fe2+ và sự oxi hóa Cu
D. sự oxi hóa Fe và sự oxi hóa Cu
1.1: Nhóm các vật liệu được chế tạo từ polime trùng ngưng là
A. nilon-6,6; tơ lapsan; thủy tinh plexiglas
B. nilon-6,6; tơ lapsan; nilon-6
C. cao su; nilon-6,6; tơ nilon
D. tơ axetat; nilon – 6,6; thủy tinh plexiglas
1.2: Chất không có khả năng tham gia phản ứng trùng ngưng là
A. axit terephtalic B. axit axetic
C. glyxin D. etylen glicol
1.3: Kim loại có các tính chất vật lý chung là:
A. Tính dẫn điện, tính dẫn nhiệt, ánh kim, tính đàn hồi.
B. Tính dẻo, tính dẫn điện, tính dẫn nhiệt, ánh kim.
Advertisements (Quảng cáo)
C. Tính dẻo, tính dẫn điện, tính khó nóng chảy, ánh kim.
D. Tính dẻo, tính dẫn điện, tính dẫn nhiệt, tính cứng.
1.4: Hợp chất X có công thức cấu tạo: CH3CH2COOCH3. Tên gọi của X là:
A. propyl axetat.
B. metyl axetat.
C. etyl axetat.
D. metyl propionat.
PHẦN RIÊNG:
PHẦN DÀNH CHO CÁC LỚP TỪ 12A1 ĐẾN 12A17
1.5: Este đơn chức X có tỷ khối hơi so với hidro là 50. Cho 10 gam X tác dụng với 200 ml dung dịch NaOH 1M (đun nóng). Cô cạn dung dịch sau phản ứng thu được 12,2 gam chất rắn khan. Công thức cấu tạo của X là (cho Na=23, C=12, H=1, O=16)
A. CH3-COO-CH=CH-CH3.
B. CH2=CH-COO-CH2-CH3.
C. CH2=CH-CH2-COO-CH3.
D. CH3-CH2-COO-CH=CH2.
1.6: Hiện tượng xảy ra khi cho đồng (II) hiđroxit vào dung dịch lòng trắng trứng:
A. Xuất hiện màu nâu.
B. Xuất hiện màu tím đặc trưng.
C. Xuất hiện màu vàng.
D. Xuất hiện màu đỏ.
1.7: Phản ứng hóa học chứng minh rằng glucozơ có chứa 5 nhóm hiđrôxyl trong phân tử là:
A. Phản ứng tráng gương và phản ứng lên men rượu
B. Phản ứng tạo 5 chức este trong phân tử
C. Phản ứng cho dung dịch màu xanh lam ở nhiệt độ phòng với Cu(OH)2
D. Phản ứng tạo kết tủa đỏ gạch với Cu(OH)2 khi đun nóng và phản ứng lên men rượu
1.8: Thủy phân hoàn toàn 13,68 gam saccarozơ rồi chia sản phẩm thành 2 phần bằng nhau.
Phần 1 cho tác dụng với lượng dư dung dịch AgNO3/NH3 thì thu được x gam kết tủa.
Phần 2 cho tác dụng với dung dịch nước brom dư, thì có y gam brom tham gia phản ứng.
Giá trị x và y lần lượt là:
A. 4,32 và 3,2 B. 8,64 và 3,2
C. 4,32 và 6,4 D. 8,64 và 6,4
1.9: Cho 12,4 gam chất X có công thức là C3H12O3N2 tác dụng với dung dịch chứa 0,3 mol NaOH đun nóng thu được hỗn hợp khí làm xanh giấy quỳ ẩm và dung dịch Y. Cô cạn dung dịch Y thu được m gam chất rắn khan. Giá trị của m là:
A. 25,2 gam B. 14,6 gam
C. 26,4 gam D. 18,6 gam
2.0: Các ion kim loại Ag+, Fe2+, Ni2+, Cu2+, Pb2+ có tính oxi hóa tăng dần theo chiều:
A. Ni2+< Fe2+< Pb2+<Cu2+< Ag+.
B. Fe2+< Ni2+< Pb2+<Cu2+< Ag+.
C. Fe2+< Ni2+< Cu2+< Pb2+< Ag+.
D. Fe2+< Ni2+< Pb2+< Ag+< Cu2+.
2.1: Tơ nilon – 6,6 là:
A. Hexaclo xiclohexan.
B. Poliamit của axit adipic và hexametylendiamin.
Advertisements (Quảng cáo)
C. Polieste của axit adipic và etylenglycol.
D. Poliamit của ε – aminocaproic.
2.2: Khi thuỷ phân este E trong môi trường kiềm (dung dịch NaOH) người ta thu được natri axetat và etanol. Vậy E có công thức là:
A. HCOOCH3.
B. CH3COOC2H5 .
C. CH3COOCH3.
D. C2H5COOCH3.
2.3: Nung bột sắt trong oxi, thu được m gam hỗn hợp chất rắn X. Hòa tan hết hỗn hợp X trong dung dịch HNO3 (dư), thoát ra 1,12 lít (ở đktc) NO (là sản phẩm khử duy nhất) và 21,78 g muối. Giá trị của m là?
A. 5,6. B. 8.
C. 4,64. D. 6.
2.4: Chất không có khả năng tham gia phản ứng trùng hợp là
A. stiren B. propen
C. isopren D. toluen
PHẦN DÀNH RIÊNG CHO CÁC LỚP TỪ 12A18 ĐẾN 12A20:
2.5: Cho một lượng kim loại M tác dụng hết với dung dịch H2SO4 loãng thu được 51,3g muối sunfat và 10,08 lít khí H2 (đktc). Kim loại M là (Mg=24; Al=27; Fe=56; Zn=65):
A. Mg B. Zn
C. Fe D. Al
2.6: Chất không phản ứng với dung dịch AgNO3/NH3, t0 tạo ra Ag là:
A. axit fomic B. fomanđehit
C. glucozơ D. axit axetic
2.7: Dãy gồm các chất được dùng để tổng hợp cao su buna–S là
A. CH2=C(CH3)-CH=CH2, C6H5-CH=CH2
B. CH2=CH-CH=CH2,CH3-CH=CH
C. CH2=CH-CH=CH2, lưu huỳnh
D. CH2=CH-CH=CH2,C6H5-CH=CH2
2.8: Dãy các ion kim loại nào sau đây đều bị Zn khử thành kim loại ?
A. Pb2+, Ag+, Al3+.
B. Cu2+, Mg2+, Pb2+.
C. Cu2+, Ag+, Na+.
D. Sn2+, Pb2+, Cu2+.
2.9: Glucozơ và mantozơ đều không thuộc loại?
A. Cacbohidrat
B. Đisaccarit
C. Monosaccarit
D. Polisaccarit
3.0: Nhóm vật liệu nào được chế tạo từ polime thiên nhiên?
A. Tơ visco, tơ tằm, cao su buna, keo dán gỗ
B. Nhựa bakelit, tơ tằm, tơ axetat
C. Cao su isopren, tơ visco, nilon-6, keo dán gỗ
D. Tơ visco, tơ tằm, phim ảnh
3.1: Cho 8,88 gam một este X có CTCT HCOOC2H5 tác dụng với 300 ml dung dịch KOH 1M. Sau phản ứng, cô cạn dung dịch thu được m gam chất rắn khan. Giá trị của m là:
A. 15,36g B. 23,52g
C. 10,08g D. 20,16g
3.2: C4H8O2 có bao nhiêu đồng phân mạch hở phản ứng được với dung dịch NaOH?
A. 5 B. 8
C. 7 D. 6
3.3: Có 3 hóa chất sau: Etylamin, phenylamin và amoniac. Thứ tự tăng dần lực bazơ được xếp theo dãy:
A. Phenylamin < Amoniac < Etylamin
B. Phenylamin < Etylamin < Amoniac
C. Amoniac < Etylamin < Phenylamin
D. Etylamin < Amoniac < Phenylamin
3.4: Phát biểu nào sau đây đúng?
A. Các amino axit đều là chất rắn ở nhiệt độ thường
B. Dung dịch của các amino axit đều không làm đổi màu quỳ tím
C. Dung dịch các amino axit đều làm đổi màu quỳ tím
D. Phân tử các amimo axit chỉ có 1 nhóm NH2 và 1 nhóm COOH
II. PHẦN TỰ LUẬNPHẦN CHUNG CHO TẤT CẢ THÍ SINH (4 điểm):
1. (1đ) Thực hiện chuỗi phản ứng sau (ghi rõ điều kiện nếu có):
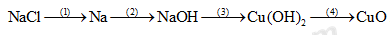
2. (1đ) Bằng phương pháp hóa học, nhận biết các dung dịch sau:
Glucozơ, fructozơ, axit axetic, hồ tinh bột
3. (1đ) Hòa tan hoàn toàn 15,4g hỗn hợp Mg và Zn bằng dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu ?
4. (1đ) Hòa tan 27,36 gam muối XSO4 vào nước được dung dịch Y. Điện phân dung dịch Y (với điện cực trơ, cường độ dòng điện không đổi) trong thời gian a giây, được m gam kim loại X duy nhất ở catot và 0,07 mol khí ở anot. Còn nếu thời gian điện phân là 2a giây thì tổng số mol khí thu được ở cả hai điện cực là 0,249 mol. Giá trị của m là ?

|
1 |
2 |
3 |
4 |
5 |
|
A |
A |
B |
A |
A |
|
6 |
7 |
8 |
9 |
10 |
|
B |
B |
B |
B |
B |
|
11 |
12 |
13 |
14 |
15 |
|
B |
B |
B |
D |
A |
|
16 |
17 |
18 |
19 |
20 |
|
B |
B |
B |
B |
B |
|
21 |
22 |
23 |
24 |
25 |
|
B |
B |
D |
D |
D |
|
26 |
27 |
28 |
29 |
30 |
|
D |
D |
D |
D |
D |
|
31 |
32 |
33 |
34 |
|
|
D |
D |
A |
A |
1.
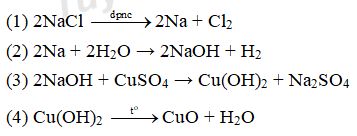
2. – Dùng quỳ tím:
+ Quỳ tím chuyển hồng: axit axetic
+ Quỳ tím không đổi màu: Glucozơ, fructozơ, hồ tinh bột
– Dùng dung dịch I2:
+ Tạo hỗn hợp có màu xanh tím đặc trưng: hồ tinh bột
+ Không tạo được hỗn hợp màu xanh tím: Glucozơ, fructozơ
– Dùng dung dịch Br2 đun nóng nhẹ:
+ Dung dịch Br2 bị mất màu: glucozo
+ Dung dịch Br2 không mất màu: fructozo
3. Đặt nMg = x mol và nZn = y mol
Mg + 2HCl → MgCl2 + H2
x → x (mol)
Zn + 2HCl → ZnCl2 + H2
y → y (mol)
Theo đề bài ta có hệ phương trình:
\(\eqalign{
& \left\{ \matrix{
{m_{hh}} = 24 + 65y = 15,4 \hfill \cr
{n_{{H_2}}} = x + y = 0,3 \hfill \cr} \right. \Rightarrow \left\{ \matrix{
x = 0,1 \hfill \cr
y = 0,2 \hfill \cr} \right. \cr
& \left\{ \matrix{
{m_{Mg}} = 0,1.24 = 2,4(g) \hfill \cr
{m_{Zn}} = 0,2.65 = 13(g) \hfill \cr} \right. \cr} \)
4. *a giây: ở catot X bị điện phân chưa hết
Catot: X2+ + 2e → X
Anot: H2O – 2e → 0,5O2 + 2H+
0,28 ← 0,07 (mol)
ne (a giây) = 0,28 mol
*2a giây: ở catot X2+ bị điện phân hết, nước đã bị điện phân
ne(2a giây) = 0,56 mol
Anot: H2O – 2e → 0,5O2 + 2H+
0,56 → 0,14 (mol)
Catot:
X2+ + 2e → X
0,171 ← 0,56–0,218 = 0,342
H2O + 1e → OH– + 0,5H2
0,218 ← 0,249–0,14 = 0,109 (mol)
=> mXSO4 = 0,171.(X + 96) = 27,36
=> X = 64 (Cu)
Khi điện phân được a giây: ne = 0,28 mol
=> nCu = 0,5ne = 0,14 mol
=> m = 0,14.64 = 8,96 gam






