Để đạt kết quả tốt trong kì thi sắp tới, Dethikiemtra gửi tới các em đề thi giữa học kì 1 lớp 9 môn Hoá học. Đề gồm 16 câu trắc nghiệm và 4 câu tự luận như sau
Kiểm tra giữa kì 1
Môn: Hóa Học 9
A. PHẦN TRẮC NGHIỆM (4 điểm)
Câu 1. Chọn câu đúng , đâu là công thức của oxit bazơ?
A. CuO,CO2, CaO B. CO2, SO2, P2O5 C. CuO, MgO, K2O D. CO2, CaO, FeO
Câu 2. Dãy nào sau đây là oxit axit?
A. CO2,SO3,P2O5 B. MgO,ZnO,CO
C. FeO, MgO, Na2O D. CO,ZnO, Al2O3
Câu 3. Đất kiềm có độ pH?
A. >7 B. <7 C. ≤ 7 D. =7
Câu 4. Dung dịch làm quỳ tím hóa xanh là?
A. NaCl B. Na2SO4 C. NaOH D. HCl
Câu 5. Cho dung dịch BaCl2 vào dung dịch Na2SO4. Phản ứng này thuộc loại:
A. Phản ứng trao đổi B. Phản ứng hoá hợp
C. Phản ứng trung hoà D. Phản ứng thế
Câu 6. Đồng Nitrat tác dụng được với?
A. FeCl2 B. ZnSO4 C. NaOH D. KCl
Câu 7. Khi nhiệt phân Fe(OH)3 ta thu được sản phẩm nào sau đây :
A. FeO và H2O B. FeO và CO2 C. Fe2O3 và H2O D. Fe2O3 và CO2
Câu 8. Muối nào sau đây tác dụng được với dung dịch NaOH?
A. CaCl2 B. CuSO4 C. BaCl2 D. K2CO3
Câu 9. Điện phân NaCl có màng ngăn, sản phẩm thu được là một trong những chất nào sau đây?
A. NaCl B. NaOH C. H2O D. Hcl
Câu 10. Kim loại nào sau đây không tác dụng với axit H2SO4 loãng?
Advertisements (Quảng cáo)
A. Fe B. Zn C. Cu D. Mg
Câu 11. Cho các cặp chất sau, cặp chất nào tác dụng được với nhau:
A. HCl với Cu B. HCl với Zn C. H2SO4 với SO2 D. H2SO4 với CO2
Câu 12. Muối nào sau đây có thể tác dụng được với dung dịch Ba(OH)2
A. NaNO3 B. CaSO4 C. KCl D. NaCl
Câu 13 : Bazơ nào sau đây là bazơ kiềm?
A. Al(OH)3 B. NaOH C. Fe(OH)3 D. Cu(OH)2
Câu 14: Dãy chất nào sau đây bị nhiệt phân hủy :
A.CaCO3, Cu(OH)2 , Fe(OH)2 C. Cu(OH)2 , CuO, NaOH
B.CaO, CaCO3 , Cu(OH)2 D. CaCO3 , NaOH, Fe(OH)3
Câu 15: Để nhận biết dd NaOH và Ba(OH)2 ta dùng hoá chất nào sau đây:
A. H2SO4 B. Hcl C. NaCl D. H2O
Câu 16 : Dãy công thức hóa học gồm toàn bộ phân bón đơn là :
A. KCl, NH4Cl, Ca3(PO4)2, KNO3. C. Ca(H2PO4)2, (NH4)2SO4, NH4Cl
B. KNO3, NH4Cl, NH4NO3, Ca3(PO4)2 D. NH4Cl, KNO3, KCl.
B. PHẦN TỰ LUẬN (6 điểm)
Advertisements (Quảng cáo)
Câu 17 (1 đ) : Hoàn thành PTHH cho sơ đồ phản ứng sau : (mỗi dấu mũi tên là một phương trình phản ứng, viết điều kiện nếu có):
![]()
Câu 18 (2đ): Nung m gam muối BaCO3 ở nhiệt độ cao, sau phản ứng thu được khí cacbonic và 45,9 gam oxit.
a. Viết phương trình hóa học.
b. Tính thể tích khí CO2 tạo thành (đktc) và m?
Câu 19 (2đ): Cho 6,5g Zn vào 200 gam dung dịch FeSO4 15,2%. Sau khi phản ứng xảy ra hoàn toàn,cho biết:
a/ Chất nào hết chất nào dư ?
b/ Tính nồng độ % của từng chất có trong dung dịch sau phản ứng ?
Câu 20(1 đ): Chỉ dùng 1 thuốc thử phân biệt các dung dịch không màu sau: H2SO4, HCl, BaCl2, NaOH.
(Biết Ba = 137, C = 12, O = 16, Ca=40, Zn=65, Fe=56, S=32)
—– HẾT —–
ĐÁP ÁN ĐỀ THI GIỮA KÌ 1 MÔN HOÁ 9
A. PHẦN TRẮC NGHIỆM
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| Đáp án | C | A | A | C | A | C | C | B | B | C | B | B | B | A | A | C |
B. PHẦN TỰ LUẬN:
Câu 17.
![]()
Câu 18.
nBaO = 45,9/153 =0,3 mol
![]()
VCO2 = 0,3.22,4 = 6,72 (lít)
m BaCO3 = 0,3.(137+ 12 + 16.3) = 59,1 (gam)
Câu 19.
nZn = 0,1 mol ; nFeSO4 = 0,2 mol
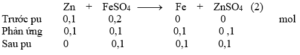
a,Zn hết, FeSO4 dư
b,Dung dịch sau pu: ZnSO4 = 0,1 mol
FeSO4 dư = 0,1 mol
mdd sau pu = 6,5 + 200 – 0,1.56 = 200,9 gam
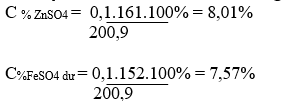
Câu 20.
– Trích mẫu thử vào từng ống nghiệm riêng biệt
– Cho quỳ tím vào từng mẫu thử:
+ Mẫu thử nào chuyển đỏ là H2SO4, HCl
+ Mẫu thử nào chuyển xanh là NaOH
+ Mẫu thử nào không chuyển màu QT là BaCl2
-Cho BaCl2 vào 2 dung dịch axit
+ Ống ngiệm nào có kết tủa là H2SO4
+ Ống nghiệm nào không có hiện tượng là HCl
![]()