Phần I. Trắc nghiệm (4đ). Hãy chọn 1 phương án đúng và ghi vào phiếu bài làm.
1. Các hạt cấu tạo nên hầu hết các nguyên tử là
A. electron và proton
B. electron và nơtron
C. proton và nơtron
D. electron, proton và nơtron
2. Số electron và số nơtron của nguyên tử lần lượt là
A. 15 và 31 B. 15 và 15
C. 16 và 15 D. 15 và 16
3.: Cho nguyên tố Ca (Z=20), cấu hình electron của Ca là
A. 1s22s22p63s23p64s1
B. 1s22s22p63s23p64s2
C. 1s22s22p63s23p64s24p1
D. 1s22s22p63s23p6
4. Nguyên tố nào sau đây là nguyên tố s ?
A. 1s22s22p3 B. 1s22s22p2
C. 1s22s22p5 D. 1s22s1
5. Nguyên tử X có cấu hình electron ở lớp ngoài cùng là 4s24p3. Vị trí của X trong bảng tuần hoàn là
A. Chu kì 4, nhóm IIIA
B. Chu kì 3, nhóm IIIA
C. Chu kì 4, nhóm VA
D. Chu kì 3, nhóm VA
6. Cấu hình electron của X là 1s22s22p63s23p4. Nhận xét nào sau đây đúng
A. X là kim loại.
B. X là phi kim.
C. X là khí hiếm
D. X vừa là một kim loại, vừa là một phi kim.
7.: Cho 2 nguyên tố X (Z=12) và Y (Z=15). Nhận định nào sau đây là đúng
A. Tính kim loại của X>Y
B.Tính kim loại của Y>X
C. Tính phi kim của X>Y
Advertisements (Quảng cáo)
D. Tính phi kim của X=Y
8.: Trong cùng một nhóm A, theo chiều điện tích hạt nhân tăng thì bán kính nguyên tử
A. không đổi
B. tăng dần
C. giảm dần
D. biến đổi không có qui luật
9.: Cho Na (Z=11) và Cl (Z=17). Liên kết trong phân tử NaCl là
A. liên kết cộng hóa trị không cực
B. liên kết cộng hóa trị có cực
C. liên kết ion
D. liên kết cộng hóa trị
10: Cộng hóa trị của cacbon và hiđro trong phân tử CH4 lần lượt là
A. 4 và 1 B. 1 và 4
C. +4 và 1- D. 4+ và 1-
11: Số oxi hóa của nitơ trong phân tử HNO3 là
A. +3 B. 3+
C. +5 D. 5+
1.2: Điện hóa trị của kali trong KCl là
A. +1 B. 1+
C. 1 D. 1-
Advertisements (Quảng cáo)
1.3: Trong phản ứng: 4NH3 + 3O2 ® 2N2 + 6H2O. Vai trò của NH3 là
A. chất khử
B. chất khử, đồng thời là chất oxi hóa
C. chất oxi hóa
D. chất cho và nhận electron.
1.4: Quá trình nào sau đây là đúng
A. \(\mathop {Al}\limits^0 + 3e \to \mathop {Al}\limits^{ + 3} \)
B. \(\mathop {Mn}\limits^{ + 7} + 4e \to \mathop {Mn}\limits^{ + 4} \)
C. \(\mathop S\limits^{ – 2} \to \mathop S\limits^0 + 2e\)
D. \(\mathop {Mn}\limits^{ + 4} + 3e \to \mathop {Mn}\limits^{ + 7} \)
1.5: Nguyên tử nào sau đây là đồng vị của
A. \({}_{17}^{37}Y\) B. \({}_{16}^{32}Z\)
C. \({}_{14}^{28}T\) D. \({}_{15}^{31}Y\)
1.6: Cacbon có 2 đồng vị: 12C và 13C. Oxi có 3 đồng vị: 16O, 17O, 18O. Số phân tử CO khác nhau được tạo nên từ các đồng vị trên là
A. 4 B. 6
C. 10 D. 12
Phần II. Tự luận (6đ).
1.7: (2,0đ)
Cân bằng phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
Zn + H2SO4 → ZnSO4 + S + H2O
1.8: (2,0đ)
Tổng số hạt trong nguyên tử X là 48 hạt. Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt.
a. Xác định số proton và số nơtron trong X?
b. Viết cấu hình electron của X? Cho biết công thức oxit cao nhất với oxi của X và công thức hợp chất khí với hiđro của X?
1.9: (2,0đ)
Hòa tan hoàn toàn 4,6 gam một kim loại R thuộc nhóm IA vào 100 gam nước, thu được 2,24 lít khí H2 (đktc)
a. Xác định tên kim loại R?
b. Tính khối lượng dung dịch thu được sau phản ứng?

|
1 |
2 |
3 |
4 |
5 |
|
D |
D |
B |
D |
C |
|
6 |
7 |
8 |
9 |
10 |
|
B |
A |
B |
C |
A |
|
11 |
12 |
13 |
14 |
15 |
|
C |
B |
A |
C |
A |
|
16 |
|
|||
|
B |
||||
II. TỰ LUẬN (6đ)
1.7: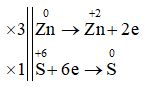
3Zn + 4H2SO4 → 3ZnSO4 + S + 4H2O
1.8: Đặt Z = số p = số e; N = số n
– Tổng số hạt trong nguyên tử X là 48 nên ta có:
Số p + số e + số n = 48 hay 2Z + N = 48 (1)
– Số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt nên ta có:
(số p + số e) – số n = 16 hay 2Z – N = 16 (2)
Từ (1) và (2) ta có hệ phương trình:
\(\left\{ \matrix{
2Z + N = 48 \hfill \cr
2Z – N = 16 \hfill \cr} \right. \to \left\{ \matrix{
Z = 16 \hfill \cr
N = 16 \hfill \cr} \right.\)
a. Số proton trong X là 16, số notron trong X là 16.
b. Cấu hình electron của 16X: 1s22s22p63s23p4
Do X có 6 electron lớp ngoài cùng nên X thuộc nhóm VIA. Vậy:
X có hóa trị VI trong oxit cao nhất với oxi => Oxit cao nhất với oxi: XO3
X có hóa trị II trong hợp chất khí với hidro => Hợp chất khí với hidro: H2X
1.9: nH2 = 2,24:22,4 = 0,1 mol
PTHH: 2R + 2H2O → 2ROH + H2
0,2 ← 0,1 (mol)
\({M_R} = \dfrac{{{m_R}} }{{{n_R}}} = \dfrac{{4,6} }{ {0,2}} = 23\) => R là Natri (Na)
b. mH2 = 0,1.2 = 0,2 (g)
Áp dụng định luật bảo toàn khối lượng, khối lượng dung dịch sau phản ứng:
m dd = mNa + mH2O – mH2 = 4,6 + 100 – 0,2 = 104,4 (g)


![[Vật Lý 10 kì 2] Hệ cô lập là gì ? Phát biểu định luật bảo toàn động lượng](https://dethikiemtra.com/wp-content/uploads/2019/04/mon-vat-ly-lop-10-1-100x75.jpg)