Dưới đây là Đề cương ôn tập thi học kì 2 lớp 8 môn Hóa học năm 2016 – 2017. Đề cương tổng hợp những dạng bài, những câu hỏi thường có trong đề thi cuối kì 2.
ÔN TẬP HỌC KÌ II – HÓAHỌC 8
NĂM HỌC : 2016-2017
DẠNG 1: TÍNH CHẤT HÓAHỌC CÁC CHẤT: KHÍ O2, KHÍ H2, NƯỚC. VIẾT PHƯƠNG TRÌNH HÓAHỌC
1. Nêu tính chất hóahọc của oxi. Ở mỗi tính chất hóahọc cho phương trình phản ứng minh họa.(xem bài tính chất của oxi)
2. Nêu tính chất hóahọc của hiđro. Mỗi tính chất viết PTHH minh họa.(xem bài tính chất- ứng dụng của H2)
3. Hoàn thành các phương trình hóahọc sau:

Câu 4: Viết các phương trình hóahọc biểu diễn các biến hóa sau:
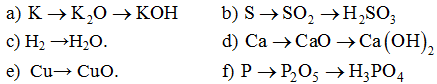
DẠNG 2: CÁC LOẠI PHẢN ỨNG HÓAHỌC VÀ CÁC LOẠI HỢP CHẤT VÔ CƠ.
1. Phản ứng hóa hợp là gì? Viết phương trình phản ứng minh họa.
(xem bài “sự oxi hóa – phản ứng hóa hợp- ứng dụng của oxi”)
2. Phản ứng phân hủy là gì? Viết phương trình phản ứng minh họa.
(xem bài điều chế oxi – phản ứng phân hủy)
3. Phản ứng thế là gì ? Viết phương trình hóa học minh họa.
4. Oxit là gì? Có mấy loại oxit chính? Mỗi loại cho 2 ví dụ.
Advertisements (Quảng cáo)
5. Axít là gì? Cho 2 ví dụ minh họa.
6. Thế nào là muối trung hòa? Thế nào là muối axit? Mỗi muối cho 2 ví dụ.
7. Đọc tên các hợp chất sau:
a) Al(OH)3 ; b) H3PO4 ; c) FeSO4 ; d) P2O5.
8. Những hợp chất có công thức hóa học sau: , , , , , , , , . Hãy cho biết mỗi loại hợp chất trên thuộc loại hợp chất nào?
9. Viết công thức hóa học và phân loại các hợp chất sau:
a) Kali clorua; b) Natri sunfit; c) Nhôm hiđrôxit; d) Axít photphoric.
e) Bari hiđroxit; f) Bạc clorua; g) Kali hiđrosunfit; h) Axit cacbonic.
i) Lưu huỳnh trioxit; j) Điphotpho pentaoxit k) Natri đihiđrophotphat;
10. Thế nào là dung dịch, dung dịch bão hòa, dung dịch chưa bão hòa? Hãy dẫn ra những thí dụ để minh họa.Thế nào là chất tan,dung môi và dung dịch.
Advertisements (Quảng cáo)
DẠNG 3: LÍ THUYẾT VÀ BÀI TẬP CƠ BẢN
1. Tìm phương pháp xác định xem trong ba lọ, lọ nào đựng dung dịch axít, lọ nào đựng dung dịch muối ăn và lọ nào đựng dung dịch kiềm (bazơ)?
2. Trong phòng thí nghiệm, dùng nguyên liệu và phương pháp gì để điều chế oxi ? Viết 2 phương trình p/ứ minh họa cho quá trình điều chế đó.
3. Trong phòng thí nghiệm dùng nguyên liệu gì để điều chế khí hiđro ? Viết phương trình p/ứ minh họa.
5. Cho 19,5g kẽm vào bình chứa dung dịch axit clohiđric.
a) Viết phương trình pứng xảy ra.
b) Tính thể tích khí hiđro (đktc) bay ra.
c) Nếu dung toàn bộ lượng khí hiddro bay ra ở trênđem khử 16g bột CuO ở nhiệt độ thích hợp ,tính khối lượng đồng thu được.
6. Cho 13g kẽm tác dụng với dung dịch có chứa 49g axit sunfuric.
a) Viết PTp/ứ xảy ra.
b) Sau p/ứ chất nào còn dư và dư bao nhiêu gam?
c) Tính khối lượng muối tạo thành và khối lượng hiđro thoát ra.
7 : Hoàn thành các phươngtrình p/ứ dưới đây và cho biết chúng thuộc loại p/ứ nào ?
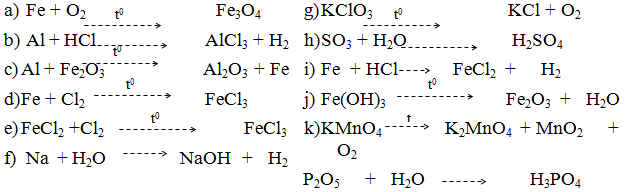
8 : Hoà tan hoàn toàn 11,2g sắt vào 100 ml dung dịch HCl 2M . Hãy :
a. Tính lượng khí H2 tạo ra ở đktc?
b. Chất nào còn dư sau p/ứ và lượng dư là bao nhiêu?
c. Nồng độ mol/l các chất sau p/ứ ?
9: Đốt cháy hoàn toàn 25,2g sắt trong bình chứa khí O2.
a. Hãy viết phương trình phảnứng xảy ra.
b. Tính thể tích khí O2 (ở đktc) đã tham gia phảnứng trên.
c. Tính khối lượng KClO3 cần dùng để khi phân huỷ thì thu được một thể tích khí O2 (ở đktc) bằng với thể tích khí O2 đã sử dụng ở phảnứng trên.
10 :Người ta cho luồng khí H2 đi qua ống đựng 2,4g bột CuO đun nóng đến khi p/ư sảy ra hoàn toàn.
a) Tính thể tích khí hiđro (đktc) vừa đủ dùng cho phảnứng trên.
b) Tính khối lượng nhôm cần dùng để khi phảnứng với axit sunfuric thì thu được lượng hiđro trên.






