
1. Oxi hóa hòa toàn 672ml (đktc) hỗn hợp hai ankan kế tiếp nhau trong cùng dãy đồng đẳng, thu được 1,8 gam H2O. Hãy đề xuất công thức phân tử của hai ankan đem dùng.
2. Một hỗn hợp A gồm hai ankan là đồng đẳng kế tiếp nhau có khối lượng 10,2 gam. Đốt cháy hoàn toàn hỗn hợp A cần 36,8 gam oxi.
a) Tính khối lượng CO2 và H2O tạo thành
b) Tìm công thức phân tử của hai ankan.
3. Khi cho CH4 phản ứng thế với clo có ánh sáng khuếch tán thì thu được một dẫn xuất của clo, trong đó clo chiếm 83,53% theo khối lượng. Xác định số nguyên tử hiđro đã bị thay thế bởi nguyên tử clo.

1. Ta có: nhỗn hợp ankan \(= \dfrac{{0,672}}{{22,4}} = 0.03\left( {mol} \right)\)
Gọi công thức tương đương của 2 ankan là: \({C_{\overline n }}{H_{2\overline n + 2}}\).
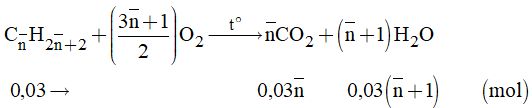
Mà:\({n_{{H_2}O}} = 0,03\left( {\overline n + 1} \right) = \dfrac{{1,8}}{{18}}\)
\(\Rightarrow \overline n = 2,33\)
Vậy công thức phân tử 2 ankan là: C2H6 và C3H8.
2. Ta có: \({n_{{O_2}}} = \dfrac{{36,8}}{{32}} = 1,15\left( {mol} \right)\)
Advertisements (Quảng cáo)
Gọi công thức tương đương của 2 ankan là: \({C_{\overline n }}{H_{2\overline n + 2}}\) có a mol.
Phản ứng cháy:
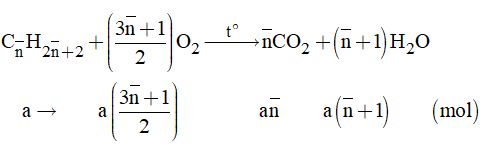
Theo đề bài, ta có hệ phương trình: \(\left\{ \begin{array}{l}{m_A} = a\left( {14\overline n + 2} \right) = 10,2\\{n_{{O_2}}} = a\left( {\dfrac{{3\overline n + 1}}{2}} \right) = 1,15\end{array} \right.\)
Giải hệ phương trình, ta được: \(\left\{ \begin{array}{l}\overline n = 3,5\\a = 0,2\left( {mol} \right)\end{array} \right.\).
a) Tính \({m_{C{O_2}}};{m_{{H_2}O}}\)
Từ (1) \( \Rightarrow {n_{C{O_2}}} = a\overline n = 0,2 \times 3,5 = 0,7\left( {mol} \right) \)
\(\Rightarrow {m_{C{O_2}}} = 0,7 \times 44 = 30,8\left( {gam} \right)\)
Advertisements (Quảng cáo)
và \({n_{{H_2}O}} = a\left( {\overline n + 1} \right) = 0,2\left( {3,5 + 1} \right) = 0,9\left( {mol} \right) \)
\(\Rightarrow {m_{{H_2}O}} = 0,9 \times 18 = 16,2\left( {gam} \right)\)
b) Lập công thức của hai ankan:
Vì hai ankan liên tiếp nhau nên \(n < \overline n < m = n + 1\)
\( \Rightarrow n < 3,5 < n + 1\)
\(\Leftrightarrow 2,5 < \overline n < 3,5\) (n là số nguyên dương)
Nghiệm duy nhất n = 3
Vậy công thức của ankan thứ nhất: C3H8 và ankan thứ hai C4H10.
3.
\[C{H_4} + xC{l_2} \to C{H_{4 – x}}C{l_x} + xHCl\]
Theo đề bài, ta có phương trình:
\(\% {m_{Cl}} = \dfrac{{35,5x}}{{16 + 35,5x}} \times 100\% = 83,53\% \)
\(\Rightarrow x = 2.\)

