
1. Cho clo tác dụng với 78 gam benzen (bột sắt làm xúc tác), thu được 78 gam clobenzen. Tính hiệu suất của phản ứng trên.
2. Cho 23 kg toluen tác dụng với hỗn hợp gồm 88 kg HNO3 66% và 74kg H2SO4 96%. Giả sử toluen và trinitrotoluen được tách hết khỏi hỗn hợp axit còn dư. Tính:
a) Khối lượng trinitrotoluen.
b) Khối lượng của hỗn hợp axit còn dư và thành phần của hỗn hợp đó.

1. Ta có: \({n_{{C_6}{H_6}}} = \dfrac{{78}}{{78}} = 1\left( {mol} \right)\)
\({C_6}{H_6} + C{l_2} \to {C_6}{H_5}Cl + HCl\left( 1 \right)\)
1\( \to \) 1 (mol)
Từ (1) \( \Rightarrow {n_{{C_6}{H_5}Cl}} = 1\left( {mol} \right)\)
Advertisements (Quảng cáo)
\(\Rightarrow {m_{{C_6}{H_5}Cl}}\)lí thuyết \( = 1 \times 112,5 = 112,5\left( {gam} \right)\)
Vậy hiệu suất phản ứng:
\(H = \dfrac{{78}}{{112,5}} \times 100\% \approx 69,33\% \)
2. Ta có: \({n_{{C_6}{H_5} – C{H_3}}} = \dfrac{{23000}}{{92}} = 250\left( {mol} \right)\)
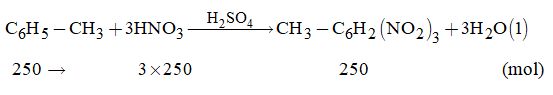
Từ (1) \( \Rightarrow \) ntrinitro toluen = 250 (mol)
Advertisements (Quảng cáo)
a) Khối lượng của trinitro toluen thu được:
\(250 \times 227 = 56750\left( {gam} \right) = 56,75\left( {kg} \right)\)
b) Khối lượng hỗn hợp axit còn dư:
\(\dfrac{{66}}{{100}} \times 88 – 47,25 + \dfrac{{96}}{{100}} \times 74 \)\(\,= 81,87\left( {kg} \right)\)
Thành phần của hỗn hợp còn lại là:
\({m_{HN{O_3}}}\)dư \( = \dfrac{{66}}{{100}} \times 88 – 47,25 = 10,83\left( {kg} \right)\)
Vì lượng H2SO4 không bị mất nên chính bằng lượng ban đầu:
\(\dfrac{{96}}{{100}} \times 74 = 71,04\left( {kg} \right)\)
Và \({m_{{H_2}O}} = \left( {88 + 74 + 23} \right)\)\(\, – \left( {56,75 + 10,83 + 71,04} \right) \)\(\,= 46,38\left( {kg} \right)\)

