Bài 1: Tìm câu đúng trong các câu sau đây:
A. Clo là chất khí không tan trong nước.
B. Clo có số oxi hóa – 1 trong mọi hợp chất.
C. Clo có tính oxi hóa mạnh hơn brom và iot.
D. Clo tồn tại trong tự nhiên dưới dạng đơn chất và hợp chất.
Chọn C.
Bài 2: Hãy nêu những phản ứng hóa học để chứng tỏ rằng clo là một chất oxi hóa rất mạnh. Vì sao có tính chất đó ?
+ Phản ứng minh họa tính oxi hóa mạnh của clo là:
Advertisements (Quảng cáo)
\(\eqalign{ & C{l_2} + {H_2}\buildrel \text{ánh sáng} \over \longrightarrow 2HCl \cr & 2Fe + 3C{l_2}\buildrel {{t^0}} \over \longrightarrow 2FeC{l_3} \cr & Cu + C{l_2}\buildrel {{t^0}} \over \longrightarrow CuC{l_2} \cr & 5C{l_2} + 2P\buildrel {{t^0}} \over \longrightarrow 2PC{l_5} \cr} \)
+ Clo có tính oxi hóa mạnh là do nó có ái lực với electron lớn, nguyên tử clo rất dễ thu thêm 1 electron để trở thành ion \(C{l^ – }\) , có cấu hình electron bền vững của khí hiếm argon (Ar).
Bài 3: Cho 69,6 g mangan đioxit tác dụng hết với dung dịch axit clohiđric đặc. Toàn bộ lượng clo sinh ra được hấp thụ hết vào 500 ml dung dịch NaOh 4M. Hãy xác định nồng độ mol của từng chất trong dung dịch thu được sau phản ứng. Coi thể tích dung dịch không thay đổi.
Ta có: \({n_{Mn{O_2}}} = {{69,6} \over {87}} = 0,8\,\,\left( {mol} \right)\)
\({n_{NaOH}} = 0,5.4 = 2\,\left( {mol} \right)\)
Advertisements (Quảng cáo)
Phản ứng:
\(\eqalign{ & Mn{O_2} + 4HC{l_{\left( \text{đặc} \right)}}\buildrel {{t^0}} \over \longrightarrow MnC{l_2} + C{l_2} \uparrow + 2{H_2}O \cr & \,\,0,8\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\, \,\,\,\,\,\,\, \;\;\;\to \,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0,8 \cr & \Rightarrow {n_{C{l_2}}} = {n_{Mn{O_2}}} = 0,8\,\,\,\left( {mol} \right) \cr} \)
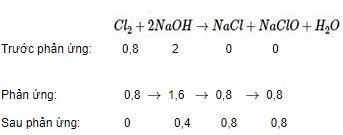
Nồng độ mol/lít của từng chất trong dung dịch sau phản ứng:
\({C_{{M_{NaCl}}}} = {C_{{M_{NaClO}}}} = {{0,8} \over {0,5}} = 1,6M;\)
\({C_{{M_{NaOH}}}} = {{0,4} \over {0,5}} = 0,8M.\)
Bài 4: Hoàn thành các phương trình hóa học dưới đây và nêu rõ vai trò của clo trong mỗi phản ứng:
\(\eqalign{ & a)\,\,FeC{l_2} + C{l_2} \to FeC{l_3} \cr & b)\,\,C{l_2} + S{O_2} + {H_2}O \to HCl + {H_2}S{O_4} \cr & c)\,\,KOH + C{l_2} \to KCl + KCl{O_3} + {H_2}O \cr & d)\,\,Ca{\left( {OH} \right)_2} + C{l_2} \to Ca{\left( {ClO} \right)_2} + CaC{l_2} + {H_2}O \cr} \)
a) \(2\mathop {Fe}\limits^{ + 2} \mathop {C{l_2}}\limits^{ – 1} + \mathop {C{l_2}}\limits^0 \to 2\mathop {Fe}\limits^{ + 3} \mathop {C{l_3}}\limits^{ – 1} \) (\(C{l_2}\) là chất oxi hóa)
b) \(\mathop {C{l_2}}\limits^0 + \mathop S\limits^{ + 4} {O_2} + 2{H_2}O \to 2H\mathop {Cl}\limits^{ – 1} \, + {H_2}\mathop S\limits^{ + 6} {O_4}\)
(\(C{l_2}\) là chất oxi hóa)
c) \(6KOH + 3\mathop {C{l_2}}\limits^0 \buildrel {{{100}^0}C} \over \longrightarrow 5K\mathop {Cl}\limits^{ – 1} + K\mathop {Cl}\limits^{ + 5} {O_3} + 3{H_2}O\)
(\(C{l_2}\) vừa là chất khử vừa là chất oxi hóa)
d) \(2Ca{\left( {OH} \right)_2} + 2\mathop {C{l_2}}\limits^0 \to Ca{(\mathop {Cl}\limits^{ + 1} O)_2} + Ca\mathop {C{l_2}}\limits^{ – 1} + 2{H_2}O\) (\(C{l_2}\) vừa là chất khử vừa là chất oxi hóa)

