Bài 3.34: a) Hãy giải thích sự liên kết giữa hai nguyên tử H tạo thành phân tử \(H_2\), giữa hai nguyên tử C1 tạo thành phân tử \(Cl_2\).
b) Thế nào là liên kết cộng hoá trị ?
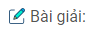
a) Nguyên tử H, với cấu hình electron là \(ls^1\), có 1 electron hoá trị. Trong phân tử \(H_2\), hai nguyên tử H liên kết với nhau bằng cách mỗi nguyên tử H góp 1 electron tạo thành một cặp electron chung :
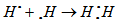
Như vậy, trong phân tử \(H_2\), mỗi nguyên tử có 2 electron giống lớp vỏ bền vững của khí hiếm heli (He).
Nguyên tử clo (Cl) có 7 electron hoá trị. Một cách tương tự, trong phân tử \(Cl_2\), mỗi nguyên tử C1 đạt được cấu hình 8 electron ở lớp ngoài cùng giống nguyên tử khí hiếm Ar khi mỗi nguyên tử góp 1 electron tạo thành cặp electron chung :
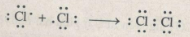
Liên kết giữa hai nguyên tử H hay giữa hai nguyên tử C1 được gọi là liên kết cộng hoá trị.
Liên kết cộng hoá trị là liên kết được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron chung [1].
[1] Thực ra, cũng có những trường hợp cá biệt, liên kết được hình thành bằng một hay một số lẻ electron.
Bài 3.35
a) Hãy biểu diễn các liên kết trong các phân tử \(H_2, Cl_2, N_2\) bằng công thức electron và bằng công thức cấu tạo.
b) Hãy cho biết thế nào là liên kết đơn, thế nào là liên kết ba, cho thí dụ.
Advertisements (Quảng cáo)
a)

b) Mỗi cặp electron chung được biểu-thị bằng một gạch nối và được coi là một liên kết.
Nếu giữa hai nguyên tử có một liên kết thì liên kết đó được gọi là liên kết đơn, thí dụ H – H ; C1 – Cl.
Nếu giữa hai nguyên tử có ba liên kết thì liên kết đó được gọi là liên kết ba, thí dụ \(N \equiv N\)
Bài 3.36
a) Thế nào là liên kết cộng hoá trị không phân cực (không cực) ?
b) Thế nào là liên kết cộng hoá trị phân cực (có cực) ? Mỗi trường hợp hãy cho hai thí dụ và biểu diễn các liên kết bằng công thức electron.
Advertisements (Quảng cáo)
a) Liên kết cộng hoá trị không phân cực là liên kết cộng hoá trị giữa hai nguyên tử có hiệu độ âm điện nhỏ hơn 0,4. Các cặp electron chung phân bố đồng đều giữa hai nguyên tử.
Thí dụ : \(H_2\) ; \(Cl_2\)
H : H ; C1 : C1
b) Liên kết cộng hoá trị phân cực (có cực) là liên kết giữa hai nguyên tử khác nhau có hiệu độ âm điện từ 0,4 đến < 1,7 ; các cặp electron phân bỏ lệch về phía nguyên tử có độ âm điện lớn.
Thí dụ: HCl ; HF
H :Cl ; H :F
Bài 3.37
Hãy giải thích sự hình thành phân tử khí cacbonic (\(CO_2\)).
Nguyên tử cacbon (C) có 4 electron hoá trị, nguyên tử oxi (O) có 6 electron hoá trị.
Trong phân tử \(\), nguyên tử c ở giữa hai nguyên tử o. Nguyên tử c góp chung với mỗi nguyên tử o hai electron, mỗi nguyên tử O góp chung với nguyên tử c hai electron tạo ra hai liên kết đôi:

Như vậy, theo công thức electron, nguyên tử c cũng như mỗi nguyên tử o đều được bao quanh bởi 8 electron lớp ngoài cùng, đạt cấu hình vững bền của khí hiếm (Ne).
Bài 3.38
Hãy viết công thức electron và công thức cấu tạo-của các phân tử \(H_2O, NH_3\) (không cần chú ý đến cấu trúc không gian).

Bài 3.39
Hãy cho biết tính chất chung của các chất có liên kết cộng hoá trị.
Liên kết cộng hoá trị là liên kết giữa các nguyên tử trong cùng một phân tử (liên kết định hướng). Như vậy, mỗi phân tử có thể được coi là một đơn vị độc lập nên so với các hợp chất ion, các hợp chất liên kết cộng hoá trị có nhiệt độ nóng chảy, nhiệt độ hoá hơi thấp.
Ở điều kiện thường, hiđro, oxi, clo, khí cacbonic ở trạng thái khí ; nước, etanol (rượu etylic) ở trạng thái lỏng ; băng phiến, iot, đường ở trạng thái rắn. Các chất có cực như etanol, đường…. dễ tan trong dung môi nước (có cực) ; các chất không cực như propan, hexan,… dễ tan trong các dung môi không cực như benzen, cacbon tetraclorua,…
Nói chung, các chất chỉ có liên kết cộng hoá trị không cực không dẫn điện ở mọi trạng thái.

