Bài 29.5: Viết các phương trình hoá học thực hiện những chuyển đổi hoá học sau
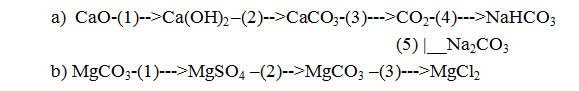

Các phương tình hóa học :
a) \((1)CaO + {H_2}O \to Ca{(OH)_2}\)
\((2)Ca{(OH)_2} + C{O_2} \to CaC{O_3} \downarrow + {H_2}O\)
\((3)CaC{O_3}\buildrel {{t^o}} \over\longrightarrow CaO + C{O_2} \uparrow \)
\((4)C{O_2} + NaOH \to NaHC{O_3}\)
\((5)C{O_2} + 2NaOH \to N{a_2}C{O_3} + {H_2}O\)
b) \((1)MgC{O_3} + {H_2}S{O_4} \to MgS{O_4} + C{O_2} \uparrow + {H_2}O\)
\((2)MgS{O_4} + N{a_2}C{O_3} \to MgC{O_3} \downarrow + N{a_2}S{O_4}\)
\((3)MgC{O_3} + 2HCl \to MgC{l_2} + C{O_2} \uparrow + {H_2}O\)
Bài 29.6: Hãy viết phương trình hoá học của các phản ứng sau
Advertisements (Quảng cáo)
(1) 2C + … ———– > 2CO
(2) Fe203 + … ———–> 2Fe + C02
(3) CO2 + … ——— > CaCO3 + H2O

\((1)2C + {O_2}\buildrel {{t^o}} \over\longrightarrow 2CO\)
\((2)F{e_2}{O_3} + 3CO\buildrel {{t^o}} \over\longrightarrow 2Fe + 3C{O_2}\)
\((3)C{O_2} + Ca{(OH)_2} \to CaC{O_3} \downarrow + {H_2}O\)
Advertisements (Quảng cáo)
Bài 29.7: Cho 19 gam hỗn hợp Na2C03 và NaHC03 tác dụng với 100 gam dung dịch HCl, sinh ra 4,48 lít khí (đktc).
Khối lượng mỗi muối trong hỗn hợp lần lượt là
A. 10,6 gam và 8,4 gam ; B. 16 gam và 3 gam ;
c. 10,5 gam và 8,5 gam ; D. Kết quả khác.

Đáp án A.
\({n_{N{a_2}C{O_3}}}:x;{n_{NaHC{O_3}}}:y;{n_{C{O_2}}} = 0,2(mol)\)
Phương trình hóa học :
\(N{a_2}C{O_3} + 2HCl \to 2NaCl + C{O_2} \uparrow + {H_2}O\)
x mol y mol
\(NaHC{O_3} + HCl \to NaCl + C{O_2} \uparrow + {H_2}O\)
y mol y mol
\(\left\{ \matrix{x + y = 0,2 \hfill \cr 106x + 84y = 19 \hfill \cr} \right. \Rightarrow x = y = 0,1\)
\({m_{N{a_2}C{O_3}}} = 0,1 \times 106 = 10,6(gam);{m_{NaHC{O_3}}} = 0,1 \times 84 = 8,4(gam)\)

