Bài 13 Luyện tập tính chất của nito, photpho và các hợp chất của chúng SBT Hóa lớp 11. Giải bài 2.50, 2.51, 2.52, 2.53 trang 20. Câu 2.50: Viết phương trình hoá học ở dạng phân tử và dạng ion rút gọn của phản ứng xảy ra trong dung dịch giữa các chất sau…; Hãy phân biệt 4 lọ không dán nhãn đựng riêng biệt từng dung dịch loãng của các chất sau : H3PO4, BaCl2, Na2CO3, (NH4)2SO4
Bài 2.50: Viết phương trình hoá học ở dạng phân tử và dạng ion rút gọn của phản ứng xảy ra trong dung dịch giữa các chất sau :
1. Bari clorua và natri photphat.
2. Axit photphoric và canxi hiđroxit, tạo ra muối axit ít tan.
3. Axit nitric đặc, nóng và sắt kim loại.
4. Natri nitrat, axit sunfuric loãng và đồng kim loại.
Phương trình hoá học ở dạng phân tử và dạng ion rút gọn của các phản ứng xảy ra trong dung dịch :
1. 3BaCl2 + 2Na3PO4 \( \to \) 6NaCl + Ba3(PO4)2\( \downarrow \)
3Ba2+ + 2\(P{O_4}^{3 – }\) \( \to \) Ba3(PO4)2\( \downarrow \)
2. \({H_3}P{O_4}\) + Ca(OH)2 \( \to \) CaHPO4\( \downarrow \) + 2H2O
\({H_3}P{O_4}\) + Ca2+ + 2\(O{H^ – }\) \( \to \) CaHPO4\( \downarrow \) + 2H2O
3. 6\(HN{O_3}\)(đặc) + Fe 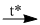 Fe(NO3)3 + 3NO2\( \uparrow \) + 3H2O
Fe(NO3)3 + 3NO2\( \uparrow \) + 3H2O
6H+ + 3\(N{O_3}^ – \) + Fe \( \to \) Fe3+ + 3NO2\( \uparrow \) + 3H2O
4. 3Cu + 4H2SO4(loãng) + 8NaNO3 \( \to \) 3Cu(NO3)2 + 2NO\( \uparrow \) + 4Na2SO4 + 4H2O
3Cu + 8H+ + 2\(N{O_3}^ – \) \( \to \) 3Cu2+ + 2NO\( \uparrow \) + 4H2O
Advertisements (Quảng cáo)
Bài 2.51: Có 4 lọ không dán nhãn đựng riêng biệt từng dung dịch loãng của các chất sau : H3PO4, BaCl2, Na2CO3, (NH4)2SO4. Chỉ được sử dụng dung dịch HCl, hãy nêu cách nhận biết chất đựng trong mỗi lọ. Viết phương trình hoá học của các phản ứng.
– Lấy một phần mỗi dung dịch vào từng ống nghiệm, rồi nhỏ dung dịch HCl vào. Ở ống nghiệm có khí thoát ra là ống đựng dung dịch Na2CO3.
Na2CO3 + 2HCl \( \to \) 2NaCl + CO2\( \uparrow \) + H2O
– Phân biệt dung dịch H3PO4, BaCl2 và (NH4)2SO4 bằng cách cho Na2CO3 tác dụng với từng dung dịch : dung dịch nào khi phản ứng cho khí thoát ra là H3PO4, dung dịch nào khi phản ứng có kết tủa trắng xuất hiện là BaCl2, dung dịch nào khi phản ứng không có hiện tượng gì là (NH4)2SO4 :
2H3PO4 + 3Na2CO3 \( \to \) 2Na3PO4 + 3CO2\( \uparrow \) + 3H2O
BaCl2 +NaCO3 \( \to \) BaCO3\( \downarrow \) + 2NaCl
Bài 2.52: Cho các chất sau : 3Ca3(PO4)2.CaF2, H3PO4, NH4H2PO4, NaH2PO4, K3PO4, Ag3PO4. Hãy lập một dãy chuyển hoá biểu diễn mối quan hệ giữa các chất đó. Viết phương trình hoá học của các phản ứng thực hiện dãy chuyển hoá trên.
Advertisements (Quảng cáo)
Dãy chuyển hoá biểu diễn mối quan hệ giữa các chất có thể là :
3Ca3(PO4)2.CaF2 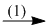 H3PO4
H3PO4 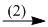 NH4H2PO4
NH4H2PO4 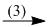 NaH2PO4
NaH2PO4 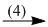 K3PO4
K3PO4 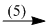 Ag3PO4
Ag3PO4
Các phương trình hoá học :
(1) 3Ca3(PO4)2.CaF2 + 10H2SO4(đặc) \( \to \) 6H3PO4 + 10CaS04\( \downarrow \) + 2HF\( \uparrow \)
(2) H3PO4 + NH3 \( \to \) NH4H2PO4
(3) NH4H2PO4 + NaOH \( \to \) NaH2P04 + NH3\( \uparrow \) + \({H_2}O\)
(4) 3NaH2PO4 + 6KOH \( \to \) Na3PO4 + 2K3PO4 + 6\({H_2}O\)
(5) K3PO4 + 3AgNO3 \( \to \) \(A{g_3}P{O_{4 \downarrow }} + 3KN{O_3}\)
Bài 2.53: Rót dung dịch chứa 11,76 g \({H_3}P{O_4}\) vào dung dịch chứa 16,8 g KOH. Sau phản ứng, cho dung dịch bay hơi đến khô. Tính khối lượng muối khan thu được.
Số mol \({H_3}P{O_4}\) : \(\frac{{11,76}}{{98}}\) = 0,12 (mol)
Số mol KOH : \(\frac{{16,8}}{{56}}\) = 0,3 (mol)
Các phản ứng có thể xảy ra :
\(\begin{array}{l}
{H_3}P{O_4} + KOH \to K{H_2}P{O_4} + {H_2}O(1)\\
{H_3}P{O_4} + 2KOH \to {K_2}HP{O_4} + 2{H_2}O(2)\\
{H_3}P{O_4} + 3KOH \to {K_3}P{O_4} + 3{H_2}O(3)
\end{array}\)
Vì tỉ lệ \({n_{KOH}}:{n_{{H_3}P{O_4}}}\) = 0,3 : 0,12 = 2,5 nằm giữa 2 và 3, nên chỉ xảy ra các phản ứng (2) và (3), nghĩa là tạo ra hai muối K2HPO4 và K3PO4.
Gọi x là số mol \({H_3}P{O_4}\) tham gia phản ứng (2) và y là số mol \({H_3}P{O_4}\) tham gia phản ứng (3) :
x + y = 0,12 (a)
Theo các phản ứng (2) và (3) tổng số mol KOH tham gia phản ứng :
2x + 3y = 0,3 (b)
Giải hộ phương trình (a) và (b) : x = 0,06 mol K2HPO4 ; y = 0,06 mol K3PO4.
Tổng khối lượng hai muối:
\({m_{{K_2}HP{O_4}}} + {m_{{K_3}P{O_4}}}\) = 0,06.174 + 0,06.212 = 10,44 + 12,72 = 23,16 (g).

