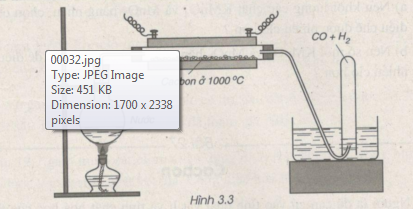
Bài 27.5: Cho hơi nước đi qua than nóng đỏ, người ta thu được hỗn hợp khí CO và H2 (hình 3.3).
a) Viết phương trình hoá học.
b) Tính thể tích hỗn hợp khí (đktc) thu được ở phản ứng trên khi dùng hết 1 tấn than chứa 92% cacbon và hiệu suất của phản ứng đạt 85%.

a) Phương trình hóa học : \(C + {H_2}O\buildrel {{t^o}} \over\longrightarrow CO + {H_2}\)
b) Thể tích hỗn hợp khí thu được.
Trong 1000 kg than có: \({{1000 \times 92} \over {100}} = 920(kg)\) cacbon
\(C + {H_2}O \to CO + {H_2}\)
12g 22,4l 22,4l
12kg 22,4\({m^3}\) 22,4\({m^3}\)
Advertisements (Quảng cáo)
\(44,8{m^3}\)
920 kg \({{44,8 \times 920} \over {12}} = 3434,7({m^3})\) hỗn hợp khí
Thể tích hỗn hợp khí thực tế thu được: \({{3434,7 \times 85} \over {100}} = 2919,5({m^3})\)
Bài 27.6: Cho 268,8 m3 hỗn hợp khí CO và H2 khử sắt(III) oxit ở nhiệt độ cao.
a) Viết phương trình hoá học.
b) Tính khối lượng sắt thu được.
Advertisements (Quảng cáo)

a) Phương trình hóa học :
\(3CO + F{e_2}{O_3}\buildrel {{t^o}} \over\longrightarrow 3C{O_2} + 2Fe(1)\)
\(3{H_2} + F{e_2}{O_3}\buildrel {{t^o}} \over\longrightarrow 3{H_2}O + 2Fe(2)\)
b) Tổng hợp (1) và (2) ta có :
Cứ 3 x 22,4 m3 hỗn hợp khí CO và H2 qua Fe203 thì thu được 2 x 56 kg Fe. 268,8 m3 hỗn hợp khí CO và H2 qua Fe203 thì thu được x kg Fe.
\(x = {{268,8 \times 2 \times 56} \over {3 \times 22,4}} = 448(kg)Fe\)
Bài 27.7: Đem nung hỗn hợp hai oxit CuO và ZnO có tỉ lệ số mol là 1 : 1 với cacbon trong điều kiện thích hợp để oxit kim loại bị khử hết, thu được hỗn hợp chất rắn X. Cho X tác dụng với dung dịch HCl dư thấy thoát ra 2,24 lít khí (ở đktc). Hãy tính khối lượng mỗi oxit kim loại.

Sơ đồ phản ứng: ZnO, CuO \(\buildrel C \over\longrightarrow \) Zn, Cu
\(Zn + 2HCl \to {H_2}\)
0,1 mol \({{2,24} \over {22,4}} = 0,1(mol)\)
Theo đề bài, ZnO, CuO có tỷ lệ số mol là 1:1 nên Zn và Cu cũng có tỉ lệ số mol 1:1 => \({n_{Cu}} = {n_{Zn}} = 0,1(mol)\).
\({m_{ZnO}} = 8,1(gam);{m_{CuO}} = 8(gam)\)

