Bài 12.1: Bạn em đã lập bảng về mối quan hệ giữa một số kim loại với một số dung dịch muối như sau
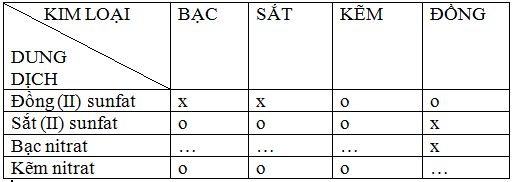
Chú thích : Dấu X là có phản ứng hoá học xảy ra.
Dấu O là không xảy ra phản ứng.
Hãy :
a) Sửa lại những dấu X và O không đúng trong các ô của bảng.
b) Bổ sung dấu X hoặc dấu O vào những dấu chấm trong các ô trống.
c) Viết các phương trình hoá học của phản ứng xảy ra theo dấu X.

ta có bảng về mối quan hệ giữa một kim loại với một số dung dịch muối:
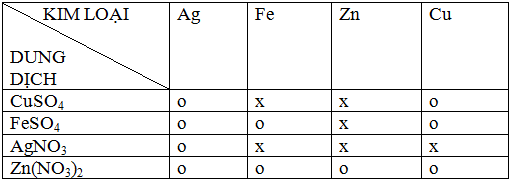
Viết các phương trình hóa học của phản ứng xảy ra theo dấu x
\(Fe + CuS{O_4} \to FeS{O_4} + Cu\)
\(Zn + CuS{O_4} \to ZnS{O_4} + Cu\)
\(Zn + FeS{O_4} \to ZnS{O_4} + Fe\)
\(Fe + 2AgN{O_3} \to Fe{(N{O_3})_2} + 2Ag\)
\(Zn + 2AgN{O_3} \to Zn{(N{O_3})_2} + 2Ag\)
\(Cu + 2AgN{O_3} \to Cu{(N{O_3})_2} + 2Ag\)
Bài 12.2: Có những chất sau : CuSO4, CuCl2, CuO, Cu(OH)2, Cu(NO3)2.
a) Hãy sắp xếp các chất đã cho thành một dãy chuyển đổi hoá học.
b) Viết các phương trình hoá học theo dãy chuyển đổi đã sắp xếp.
Advertisements (Quảng cáo)

a) Hướng dẫn
Có nhiều cách sắp xếp các chất đã cho thành các dãy chuyển đổi hoá học. miễn sao từ chất đứng trước có thể điều chê trực tiếp chất đứng sau. Thí dụ :
CuSO4 —> CuCl2 —> Cu(OH)2 —> CuO —> Cu(NO3)2.
Cu(OH)2 —> CuO —> CuSO4 —> CuCl2 —> Cu(NO3)2.
Các phương trình hoá học của dãy biến hoá (1) :
CuSO4 + BaCl2 —> BaSO4 \( \downarrow \) + CuCI2
CuCl2 + 2NaOH —> 2NaCl + Cu(OH)2
Cu(OH)2 \(\buildrel {{t^o}} \over\longrightarrow\) CuO + H2O
CuO + 2HNO3 —> Cu(NO3)2 + H2O
Các phương trình hoá học của dãy biến hoá (2) (không có ở dãy (1)) :
CuO + H2SO4 —> CuSO4 + H2O
CuCI2 + 2AgNO3 —> 2AgCl \( \downarrow \) + Cu(NO3)2
Bài 12.3: Có 5 ống nghiệm A, B, c, D, E. Mỗi ống có chứa 12,4 gam đồng(II) cacbonat CuCO3. Khi đun nóng, muối này bị phân huỷ dần :
Advertisements (Quảng cáo)
CuCO3(r) \(\buildrel {{t^o}} \over\longrightarrow \) CuO(r) + CO2 (k)
Mỗi ống được nung nóng, đế nguội và cân chất rắn còn lại trong ống nghiệm. Sau đó, thí nghiệm trên lại được lạp lại 3 lần nữa để CuCO3 bị phân huỷ hết. Các kết quả được ghi lại như sau :
|
ỐNG NGHIỆM |
KHỐI LƯỢNG CHẤT RẮN sau Mồl lần nung (gam) |
|||
|
|
Lần thứ 1 |
Lần thứ 2 |
Lần thứ 3 |
Lần thứ 4 |
|
A |
8,6 |
8,5 |
8,0 |
8,0 |
|
B |
9,8 |
9,5 |
8,5 |
8,0 |
|
C |
16,0 |
9,7 |
9,1 |
8,5 |
|
D |
8,0 |
8,0 |
8,0 |
8,0 |
|
E |
12,4 |
12,4 |
12,4 |
12,4 |
a) Hãy dùng những kết quả ở bảng trên để trả lời những câu hỏi sau :
1. Ống nghiệm nào đã bị bỏ quên, không đun nóng ?
2. Ống nghiệm nào có kết quả cuối cùng dự đoán là sai ? Vì sao ?
3. Vì sao khối lượng chất rắn trong ống nghiêm A là không đổi sau lần nung thứ 3 và thứ 4 ?
4. Ống nghiệm nào mà toàn lượng đồng(II) cacbonat đã bị phân huỷ sau lần nung thứ nhất ?
b) Hãy tính toán để chứng minh kết quả thí nghiệm của những ống nghiệm nào là đúng.

a) 1. Ống nghiệm E (khối lượng CuCO3 không thay đổi).
2. Ống nghiệm C, vì khác với các kết quả của những ống nghiệm A, B, D.
3. Sau lần nụng thứ 3 thì toàn lượng CuCO3 đã bị phân huỷ hết thành CuO.
4. Ống nghiệm D.
b) Phần tính toán :
Theo phương trình hoá học :
124 gam CuCO3 sau khi bị phân huỷ sinh ra 80 gam CuO.
Vậy 12,4 gam CuCO3 sau khi bị phân huỷ sinh ra :
\({m_{CuO}} = {{80 \times 12,4} \over {124}} = 8,0(gam)\)
Thí nghiệm được tiến hành trong các ống nghiệm A, B, D là đúng.
Bài 12.4: Dẫn ra những phản ứng hoá học để chứng minh rằng
a) Từ các đơn chất có thể điều chế hợp chất hoá học.
b) Từ hợp chất hoá học có thể điều chế các đơn chất.
c) Từ hợp chất hoá học này có thể điều chế hợp chất hoá học khác

Hướng dẫn
a) Thí dụ, từ hai đơn chất Na và Cl2 có thể điều chế hợp chất NaCl.
b) Từ hợp chất H2O bằng phương pháp điện phân có thể điều chế các đơn chất là H2 và O2.
c) Từ hợp chất bazơ Cu(OH)2 có thể điều chế hợp chất oxit CuO bằng phươnu pháp nhiệt phân. Hoặc từ muối CaCO3 có thể điều chế các oxit CaO, CO2.

