Bài 1.47: Hãy cho biết số electron tối đa có thể phân bố trên :
Phân lớp s.
Phân lớp p.
Phân lớp d.
Phân lớp f.
Hãy cho nhận xét về quy luật của các số electron tối đa đó.
Số electron tối đa có thể phân bố trên :
Phân lớp s : 2.
Phân lớp p : 6.
Phân lớp d : 10.
Phân lớp f : 14.
Nhận xét: Số electron tối đa trên các phân lớp s, p, d, f gấp 2 lần các số lẻ liên tiếp 1, 3, 5, 7.
Bài 1.48: a) Hãy cho biết quan hệ giữa số nguyên n đặc trưng cho các lớp và số electron tối đa trên lớp tương ứng.
b)Hãy cho biết số electron tối đa trên các lớp K, L, M.
c)Tượng trưng mỗi lớp electron bằng một đường tròn và mỗi electron bằng một chấm, hãy vẽ sơ đồ mô tả số electron tối đa trên các lớp K, L, M.
a) Một cách vắn tắt người ta nói lớp n có tối đa 2n2 electron.
b) Số electron tối đa trên lớp K (n=1) là 2.12
Số electron tối đa trên lớp L (n=2) là 2.22=8
Số electron tối đa trên lớp M (n=3) là 2.32=18
Advertisements (Quảng cáo)
c) Sơ đồ như hình vẽ :
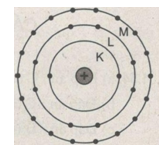
(Lớp K có tối đa 2 electron, lớp L có tối đa 8 electron, lớp M có tối đa 18 electron).
Bài 1.49: Hãy viết các kí hiệu của các phân lớp thuộc lớp M theo thứ tự tăng dần của các mức năng lượng tương ứng.
Lớp M (n = 3) có 3 phân lớp, năng lượng tăng dần từ 3s đến 3d : 3s, 3p, 3d.
Bài 1.50: Nguyên tử của nguyên tố X có tổng số 3 electron trong lớp M. Xác định nguyên tố X.
Advertisements (Quảng cáo)
Cách 1 : Lớp M (lớp thứ 3) có 3e → cấu hình e lớp M là : \(3s^23p^1\) —> cấu hình e đầy đủ của X : \(ls^22s^22p^63s^23p^1\) \(Z_X\) = 13 -> X : Al
Cách 2 : Lớp M (lớp thứ 3) có 3e → cấu hình e lớp M là : \(3s^23p^1\) , lớp M chưa bão hòa e → M là lớp ngoài cùng → X có 3 lớp e → X thuộc chu kì 3 (STT chu kì = số lớp e), nhóm IIIA (STT nhóm = số e hoá trị, e cuối cùng được xếp vào phân lớp p nên X thuộc nhóm chính (nhóm A)) → X : Al.
Bài 1.51: Vỏ electron của nguyên tử một nguyên tố A có 20e. Hãy cho biết :
+ Nguyên tử có bao nhiêu lớp e ?
+ Lớp ngoài cùng có bao nhiêu e ?
+ A là kim loại hay phi kim ? Xác định tên nguyên tố A.
Cấu hình e của nguyên tử A : \(ls^22s^22p^63s^23p^64s^2\).
→ Nguyên tử A có 4 lớp e. Có 2 e ở lớp ngoài cùng (lớp thứ 4) → là kim loại (những nguyên tử có từ 1 đến 3 e ở lớp ngoài cùng), \(Z_A\) = 20 → A là Ca.
Bài 1.52: Nguyên tố A có cấu hình e lớp ngoài cùng là \(4s^1\), nguyên tố B có phân lớp e cuối là \(3p^2\). Viết cấu hình đầy đủ và xác định tên nguyên tố A, K.
Nguyên tố A là một trong ba trường hợp sau :
Nguyên tố B là silic : \(1{{\rm{s}}^2}2{{\rm{s}}^2}2{p^6}3{s^2}3{p^2}\) (Z=14)
Bài 1.53: Nguyên tử của nguyên tố X có tổng số hạt electron trong các phân lớp p là 7. Một nguyên tử của nguyên tố Y có số hạt mang điện nhiều hơn số hạt mang điện của một nguyên tử X là 8 hạt. Xác định X, Y.
X : Các phân lớp p của X có 7 e → có 2 phân lớp p →\(2p^6\) và \(3p^1\)
→ Cấu hình e của X :\( ls^22s^22p^63s^23p^1\) → z = 13 (Al)
Số hạt mang điện của X là \(2Z_X\) = 26 → Số hạt mang điện của Y : 26 + 8 = 34 → \(Z_Y\) = 17 (Cl).

