Bài trắc nghiệm 3.11, 3.12
3.11. Natri silicat có thể được tạo thành bằng cách
A. đun SiO2 với NaOH nóng chảy.
B. cho SiO2 tác dụng với dung dịch NaOH loãng.
C. cho dung dịch K2SiO3 tác dụng với dung dịch NaHCO3.
D. cho Si tác dụng với dung dịch NaCl.
3.12. Silic và nhôm đều phản ứng được với dung dịch các chất trong dãy nào sau đây ?
A. HCl, HF
B. NaOH, KOH
C. Na2CO3, KHCO3
D. BaCl2, AgNO3
3.11. A
3.12. B
Bài 3.13: Hoàn thành các phương trình hóa học sau ( ghi rõ điều kiện phản ứng, nếu có ) :
1. \(Si + {X_2} \to \)
\({X_2}\) là \({F_2},C{l_2},B{{\rm{r}}_2}.\)
Advertisements (Quảng cáo)
2. \(Si + {O_2} \to \)
3. \(Si + Mg \to \)
4. \(Si + KOH + ? \to {K_2}Si{O_3} + ?\)
5. \(Si{O_2} + NaOH \to \)
1. \(Si + 2{F_2} \to Si{F_4}\)
\(Si + 2C{l_2}\)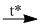 \(SiC{l_4}\)
\(SiC{l_4}\)
\(Si + 2B{r_2}\)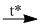 \(SiB{r_4}\)
\(SiB{r_4}\)
2. \(Si + {O_2}\)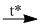 \(Si{O_2}\)
\(Si{O_2}\)
3. \(Si + 2Mg\)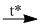 \(M{g_2}Si\)
\(M{g_2}Si\)
Advertisements (Quảng cáo)
4. \(Si + 2KOH + {H_2}O \to {K_2}Si{O_3} + 2{H_{2 \uparrow }}\)
5. \(Si{O_2} + 2NaOH\)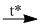 \(N{a_2}Si{O_3} + {H_2}O\)
\(N{a_2}Si{O_3} + {H_2}O\)
Bài 3.14: Cho các chất sau đây : silic, silic đioxit, axit silixic, natri silicat, magie silixua. Hãy lập thành một dãy chuyển hoá giữa các chất trên và viết các phương trình hoá học.
Dãy chuyển hoá có thể là
Mg2Si  Si
Si  SiO2
SiO2  Na2SiO3
Na2SiO3  H2SiO3
H2SiO3
Các phương trình hoá học có thể là :
(1) Si + 2Mg 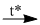 Mg2Si
Mg2Si
(2) Si + O2 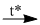 SiO2
SiO2
(3) SiO2 + 2NaOH(nóng chảy) 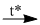 Na2SiO3 + H2O
Na2SiO3 + H2O
(4) Na2SiO3 + 2HCl \( \to \) H2SiO3\( \downarrow \) + 2NaCl
Bài 3.15: Có a gam hỗn hợp X gồm Si và Al tác dụng với dung dịch NaOH dư, thu được 1,792 lít hiđro. Mặt khác, cũng lượng hỗn hợp X như trên khi tác dụng với dung dịch HCl dư, thu được 0,672 lít hiđro.
Tính a, biết rằng các thể tích khí đều được đo ở đktc và Al tác dụng với dung dịch NaOH theo phản ứng :
2Al + 2NaOH + 2H2O \( \to \) 2NaAlO2 + 3H2\( \uparrow \)
– Si và Al phản ứng với dung dichj NaOH :
\(Si + 2NaOH + {H_2}O \to N{a_2}Si{O_3} + 2{H_{2 \uparrow }}\) (1)
\(2l + 2NaOH + 2{H_2}O \to 2NaAl{O_2} + 3{H_{2 \uparrow }}\) (2)
– Khi X tác dụng với HCl, chỉ có Al tham gia phản ứng :
\(2Al + 6HCl \to 2AlC{l_3} + 3{H_{2 \uparrow }}\) (3)
Theo (3) : \({n_{Al}} = \frac{2}{3}.{n_{{H_2}}} = \frac{2}{3}.\frac{{0,672}}{{22,4}} = 0,02(mol)\)
Khối lượng Al trong hỗn hợp X là : 0,02.27 = 0,54 (g).
Theo (2) : \({n_{{H_2}}} = \frac{3}{2}.{n_{Al}} = \frac{3}{2}.0,02 = 0,03(mol)\)
Theo (1) : \({n_{Si}} = \frac{1}{2}.{n_{{H_2}}} = \frac{1}{2}.(\frac{{1,792}}{{22,4}} – 0,03) = 0,025(mol)\)
Khối lượng Si trong hỗn hợp X là : 0,025.28 = 0,7 (g)
\(a = {m_{Al}} + {m_{Si}} = 0,54 + 0,7 = 1,24(g)\)

