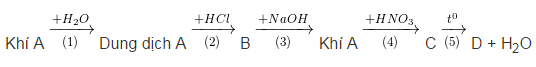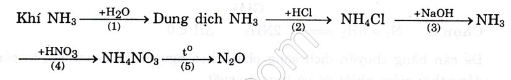[Bài 8 hóa học 11] giải bài 1, 2, 3 trang 37; bài 4, 5, 6, 7, 8 trang 38 SGK Hóa lớp 11: Amoniac và muối amoni – Chương 2.
Bài 1. Mô tả và giải thích hiện tượng xảy ra trong thí nghiệm chứng minh rằng ammoniac tan nhiều trong nước.
Giải bài 1: Nạp đầy khí NH3 vào bình thủy tinh trong suốt, đậy bình bằng ống cao su có ống thủy tinh vuốt nhọn xuyên qua. Nhúng dần ống thủy tinh vào một chậu thủy tinh chứa nước có pha vài giọt dung dịch phenolphtalein, ta thấy nước trong chậu phun vào bình thành những tia màu hồng. Đó là do khí NH3 tan nhiều trong nước làm giảm áp suất trong bình và nước bị hút vào bình. Tia nước có màu hồng chứng tỏ dung dịch có tính bazơ
Bài 2. Hoàn thành sơ đồ chuyển hóa sau đây và viết các phương trình hóa học:
Biết rằng A là hợp chất của nitơ.
Giải bài 2: Chọn A: NH3; B: NH4Cl; C: NH4NO3; D: N2
PTHH:
Bài 3. Hiện nay, để sản xuất ammoniac, người ta điều chế nitơ và hiđro bằng cách chuyển hóa có xúc tác một hỗn hợp gồm không khí, hơi nước và khí metan (thành phần chính của khí thiên nhiên). Phản ứng giữa khí metan và hơi nước tạo ra hiđro và cacbon đioxit. Để loại khí oxi và thu khí nitơ, người ta đốt khí metan trong một thiết bị kín chứa không khí.
Hãy viết các phương trình hóa học của phản ứng điều chế hiđro, loại khí oxi và tổng hợp khí ammoniac.
Đáp án bài 3: CH4 + 2H2O →t0,xt CO2 + 4H2
CH4 + 2O2 (kk) →t0 CO2 + 2H2O nên còn lại N2
Advertisements (Quảng cáo)
N2 + 3H2 ⇔ 2NH3
Bài 4: Trình bày phương pháp hóa học để phân biệt các dung dịch: NH3, Na2SO4, NH4Cl, (NH4)2SO4. Viết phương trình hóa học của các phản ứng đã dùng.
Hướng dẫn: Để phân biệt các dung dịch: NH3, Na2SO4, NH4Cl, (NH4)2SO4, có thể dùng thuốc thử lần lượt là: dd BaCl2, dd NaOH.
Bài 5. Muốn cho cân bằng của phản ứng tổng hợp amoniac chuyển dịch sang phải, cần phải đồng thời:
A. Tăng áp suất và tang nhiệt độ.
B. Giảm áp suất và giảm nhiệt độ.
C. Tăng áp suất và giảm nhiệt độ.
D. Giảm áp suất và tang nhiệt độ.
Chọn đáp án C
Advertisements (Quảng cáo)
Bài 6 trang 38: Trong phản ứng nhiệt phân các muối NH4NO2 và NH4NO3, số oxi hóa của nitơ biến đổi như thế nào ? Nguyên tử nitơ trong ion nào của muối đóng vai trò chất khử và nguyên tử nitơ trong ion nào của muối đóng vai trò chất oxi hóa ?
Giải bài 6: NH4NO2 →t0 N2 + 2H2O;
NH4NO3 →t0 N2O + 2H2O
N có số oxi hóa +3 và +5 trong NO2– và NO3– : đóng vai trò chất oxi hóa.
N có số oxi hóa -3 trong NH4+: đóng vai trò chất khử.
Bài 7. ( Hóa 11 trang 38) Cho dung dịch NaOH dư vào 150,0 ml dung dịch (NH4)2SO4 1,00 M, đun nóng nhẹ.
a) Viết phương trình hóa học ở dạng phân tử và dạng ion rút gọn.
b) Tính thể tích khí (đktc) thu gọn.
Đáp án: a) n(NH4)2S04 = 0.15 . 1 = 0.15 mol => nNH+ = 0.3 mol
(NH4)2S04 + 2NaOH -> Na2S04 + 2NH3↑ + 2H20
NH4+ + OH– -> NH3↑ + H20
0,3 mol 0,3 mol
Vậy VNH3 = 0,3.22,4 = 6,72l
b) Thể tích NH3 thu được (đktc): 6,72 lít.
Bài 8. Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,0 gam NH3 ? Biết rằng hiệu suất chuyển hóa thành amoniac là 25,0 %. Các thể tích khí được đo ở đktc.
A. 44,8 lít N2 và 134,4 lít H2
B. 22,4 lít N2 và 134,4 lít H2
C. 22,4 lít N2 và 67,2 lít H2
D. 44,8 lít N2 và 67,2 lít H2
Chọn A
Do hiệu suất 25 % nên thể tích N2, H2 cần gấp 4 lần so với lí thuyết.