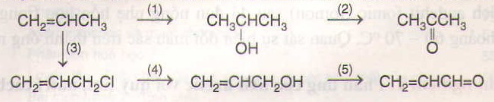
Bài 6: Viết phương trình hóa học của các phản ứng hoàn thành dãy chuyển hóa sau:
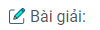
+ Các điều kiện phản ứng
(1) Cộng H2O/xt H+ ; (2) oxi hóa, ví dụ bằng CuO ; (3) tác dụng với clo, ở 4500C ; (4) thủy phân trong môi trường bazơ ; (5) oxi hóa, ví dụ bằng CuO.
Bài 7: Hợp chất X có công thức phân tử C3H6O tác dụng với một lượng dư AgNO3 trong dung dịch NH3. Công thức nào sau đây là công thức cấu tạo của X.

 D. CH3CH2CH=O.
D. CH3CH2CH=O.
Bài 8: Cho dung dịch chứa 0,58 gam chất hữu cơ X tác dụng với một lượng dư AgNO3 trong dung dịch NH3 thu được 2,15 gam kết tủa.
Advertisements (Quảng cáo)
Xác định công thức phân tử, viết công thức cấu tạo và gọi tên của hợp chất X>
– X là anđehit đơn chức
RCHO + 2AgNO3 + 3NH3 + H2O → RCOONH4 + 2Ag + 2NH4NO3
nAg = 0.02 mol => nRCHO = \(\frac{1}{2}\) nAg = 0,01 mol
Advertisements (Quảng cáo)
MRCHO = 58,0 g/mol. R là C2H5 , X là CH3CH2CHO.
Bài 9: Axit fomic tác dụng với AgNO3 trong dung dịch NH3 tạo ra kết tủa bạc kim loại. Dựa vào cấu tạo phân tử của axit fomic để giải thích, viết phương trình hóa học của phản ứng.
Cấu tạo của phân tử axit có nhóm –CHO.
Bài 10: Dẫn hơi của 3 gam etanol vào trong ống sứ nung nóng chứa bột CuO dư. Làm lạnh để ngưng tụ sản phẩm hơi đi ra khỏi ống sứ được chất lỏng A. Khi A phản ứng hoàn toàn với một lượng dư dung dịch AgNO3 trong NH3 thấy có 8,1 gam bạc kết tủa.
Tính hiệu suất của quá trình oxi hóa etanol?
C2H5OH + CuO → CH3CHO + Cu + H2O
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag + 2NH4NO3
nCH3CHO = \(\frac{1}{2}\) nAg = \(\frac{1}{2}\) . \(\frac{8,1}{108}\) = 0,0375 mol.
nC2H5OH = \(\frac{3}{46}\) mol
Hiệu suất của phản ứng oxi hóa etanol :
\(\frac{0,0375}{3,00}\) . 46. 100% = 57,5 %.

