Bài 19.5: Ở Việt Nam có những loại quặng sắt nào ? Viết công thức hoá học và cho biết địa điểm của những loại quặng đó.

Ở Việt Nam có loại quặng hematit (Fe203) ở Trại Cau, tỉnh Thái Nguyên.. Vì vậy, nước ta đã xây dựng khu công nghiệp gang – thép ở Thái Nguyên…
Bài 19.6: Viết các phương trình hoá học thực hiện dãy chuyển đổi hoá học sau
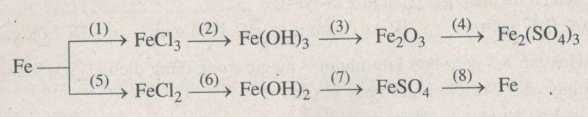

\((1)2Fe + 3C{l_2}\buildrel {{t^o}} \over\longrightarrow 2FeC{l_3}\)
\((2)FeC{l_3} + 3NaOH \to Fe{(OH)_3} \downarrow + 3NaCl\)
\((3)2Fe{(OH)_3}\buildrel {{t^o}} \over\longrightarrow F{e_2}{O_3} + 3{H_2}O\)
\((4)F{e_2}{O_3} + 3{H_4}S{O_4} \to F{e_2}{(S{O_4})_3} + 3{H_2}O\)
\((5)Fe + 2HCl \to FeC{l_2} + {H_2} \uparrow \)
\((6)FeC{l_2} + 2NaOH \to Fe{(OH)_2} \downarrow + 2NaCl\)
Advertisements (Quảng cáo)
\((7)Fe{(OH)_2} + {H_2}S{O_4} \to FeS{O_4} + 2{H_2}O\)
\((8)FeS{O_4} + Zn \to ZnS{O_4} + Fe \downarrow \)
Bài 19.7: Có hỗn hợp bột kim loại gồm sắt và đồng. Trình bày phương pháp tách riêng mỗi kim loại.
Trả lời
Cho hỗn hợp bột kim loại sắt và đồng vào dung dịch HCl, đồng không tác dụng. Đem lọc hỗn hợp sau phản ứng, ta được đồng và dung dịch nước lọc.
Cu + HCl ——–> không phản ứng.
Fe + 2HCl ———–> FeCI2 + H2.
Advertisements (Quảng cáo)
Cho Zn vào dung dịch nước lọc, sau phản ứng thu được Fe :
Zn + FeCl2 ———-> ZnCl2 + Fe
Bài 19.8: Cho các kim loại sau : đồng, sắt, nhôm, bạc. Cho biết các kim loại thoả mãn những trường hợp sau
a) Không tan trong dung dịch axit clohiđric và dung dịch axit suníuric loãng.
b) Tác dụng được với dung dịch axit và dung dịch kiềm.
c) Đẩy được đồng ra khỏi dung dịch muối đồng.

a) Đồng, bạc không tan trong dung dịch HCl và dung dịch H2S04 loãng.
b) Nhôm tan được trong dung dịch axit và dung dịch kiềm.
2Al + 6HCl ———> 2AlCl3 + 3H2
2Al + 2NaOH + 2H20 ———–> 2NaAl02 + 3H2
c) Sắt và nhôm đẩy được đồng ra khỏi dung dịch muối đồng :
Fe + CuS04 ———> FeS04 + Cu
2Al + 3CuS04 ——— > Al2(S04)3 + 3Cu

