Bài 5.21: Viết công thức cấu tạo của :
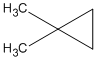
1. 1,1-đimetylxiclopropan;
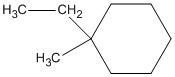
2. 1-etyl-1-metylxiclohexan;
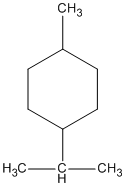
3. 1-metyl-4-isopropylxiclohexan.
1. 
2. 
3. 
Bài 5.22: Một monoxiclohexan có tỉ khối hơi so với nitơ bằng 3.
1. Xác định công thức phân tử của xicloankan đó.
2. Viết công thức cấu tạo và tên tất cả các xicloankan ứng với công thức phân tử tìm được.
1. \(\begin{array}{l}
{C_n}{H_{2n}} = 28.3 = 84\\
14n = 84 \Rightarrow n = 6
\end{array}\)
CTPT: \({C_6}{H_{12}}\)
Các CTCT:
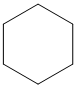
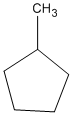
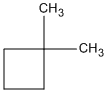
xiclohexan metylxiclopentan 1,1-đimetylxiclobutan
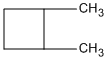
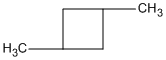
1,2-đimetylxiclobutan 1,3 đimetyl xiclobutan
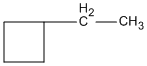
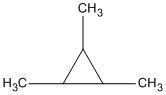
etylxiclobutan 1,2,3-trimetylxiclopropan
Advertisements (Quảng cáo)
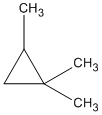
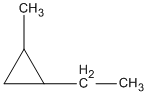
1,1,2-trimetylxiclopropan 1-etyl-2-metylxiclopropan
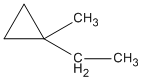
1-etyl-1-metylxiclopropan
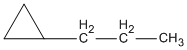
propylxiclopropan
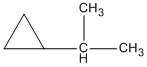
isopropylxiclopropan
Bài 5.23: Hỗn hợp khí A chứa một ankan và một monoxicloankan. Tỉ khối của A đối với hiđro là 25,8. Đốt cháy hoàn toàn 2,58 g A rồi hấp thụ hết sản phẩm cháy vào dung dịch Ba(OH)2 dư, thu được 35,46 g kết tủa.
Xác định công thức phân tử và phần trăm thể tích của từng chất trong hỗn hợp khí A.
Giả sử trong 2,58 g hỗn hợp A có X mol \({C_n}{H_{2n + 2}}\) (n > 1) và y mol \({C_m}{H_{2m}}\) (m > 3). Vì \(\overline {{M_A}} \) = 25,8 X 2 (g/mol) nên :
\(x + y = \frac{{2,58}}{{25,8.2}} = 0,05(1)\)
\({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
Advertisements (Quảng cáo)
x mol nx mol
\({C_m}{H_{2m}} + \frac{{3n}}{2}{O_2} \to mC{O_2} + m{H_2}O\)
y mol my mol
\(C{O_2} + Ba{(OH)_2} \to BaC{O_3} \downarrow + {H_2}O\)
SỐ mol C02 = SỐ mol BaC03= \(\frac{{35,46}}{{197}}\) = 0,18 (mol)
nx + my = 0,18 (2)
Khối lượng hỗn hợp A :
(14n + 2)x + 14my = 2,58 (3)
\( \Rightarrow \) 14(nx + my) + 2x = 2,58 => 2x = 2,58 – 14 X 0,18
\( \Rightarrow \) x = 0,03 ; y = 0,05 – 0,03 = 0,02
Thay giá trị của x và y vào (2) ta có
0,03n + 0,02m = 0,18
3n + 2m = 18
3n = 18 – 2m
n = 6 – \(\frac{{3m}}{2}\)
Nghiệm thích hợp là m = 3 ; n = 4.
Nghiệm m = 6 và n = 2 phải loại vì C6H12 là chất lỏng (ts = 81°C).
% về thể tích của C4H10 : \(\frac{{0,03}}{0,05}\). 100% = 60,0%
% về thể tích của C3H6 : 100% – 60% = 40,0% thể tích hỗn hơp A.
Bài 5.24: Chất khí A là một xicloankan. Khi đốt cháy 672 ml A (đktc), thì thấy khối lượng C02 tạo thành nhiều hơn khối lượng nước tạo thành 3,12 g.
1. Xác định công thức phân tử chất A.
2. Viết công thức cấu tạo và tên các xicloankan ứng với công thức phân tử tìm được.
3. Cho chất A qua dung dịch brom, màu của dung dịch mất đi. Xác định công thức cấu tạo đúng của chất A.
1. \({C_n}{H_{2n}} + \frac{{3n}}{2}{O_2} \to nC{O_2} + n{H_2}O\)
Khi đốt 1 moi CnH2n, khối lượng C02 nhiều hơn khối lượng nước 26n gam.
Khi đốt 0,03 mol CnH2n, khối lượng C02 nhiều hơn khối lượng nước 3,12 g.
\(\frac{1}{{0,03}} = \frac{{26n}}{{3,12}} \Rightarrow n = 4\)
CTPT của khí A là \({C_4}{H_8}\)
2. Các CTCT

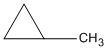
xiclobutan metylxiclopropan
3. Chất A làm mất màu nước brom, vậy A phải có vòng ba cạnh, chất A là metylxiclopropan.

