Bài 24 Luyện tập hợp chất hữu cơ, công thức phân tử và công thức cấu tạo SBT Hóa lớp 11. Giải bài 4.33, 4.34, 4.35 trang 33, 34. Câu 4.33: Trong số các chất hữu cơ đã được học ở lớp 9, hãy kể ra 2 cặp chất có công thức phân tử khác nhau nhưng có cùng công thức đơn giản nhất…; Viết công thức cấu tạo của 2 chất có cùng công thức phân tử C4H10 và của 2 chất có cùng công thức phân tử C2H60 ?
Bài 4.32. Trong số các chất hữu cơ đã được học ở lớp 9, hãy kể ra 2 cặp chất có công thức phân tử khác nhau nhưng có cùng công thức đơn giản nhất.
2. Viết công thức cấu tạo của 2 chất có cùng công thức phân tử C4H10 và của 2 chất có cùng công thức phân tử C2H60.
1. Axetilen C2H2 và benzen C6H6 có cùng công thức đơn giản nhất là CH.
Axit axetic C2H402 và glucozơ C6H1206 có cùng công thức đơn giản nhất là CH20.
2. CH3 – CH2 – CH2 – CH3 và 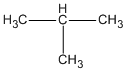 ;
;
CH3 – CH2 – OH và CH3 – O – CH3.
Bài 4.33. Hợp chất hữu cơ A có thành phần khối lượng của các nguyên tố như sau : C chiếm 24,24% ; H chiếm 4,04% ; Cl chiếm 71,72%.
1. Xác định công thức đơn giản nhất của A.
2. Xác định công thức phân tử của A biết rằng tỉ khối hơi của A đối với C02 là 2,25.
3. Dựa vào thuyết cấu tạo hoá học, hãy viết các công thức cấu tạo mà chất A có thể có ở dạng khai triển và dạng thu gọn.
1. Chất A có dạng CxHyClz
x : y : z = \(\frac{{24,24}}{{12}}:\frac{{4,04}}{1}:\frac{{71,72}}{{35,5}}\) = 2,02 : 4,04 : 2,02 = 1 : 2 : 1
Công thức đơn giản nhất là CH2Cl.
2. MA = 2,25.44,0 = 99,0 (g/mol)
(CH2Cl)n= 99,0 \( \Rightarrow \) 49,5n = 99,0 \( \Rightarrow \) n = 2
CTPT là C2H4Cl2.
Advertisements (Quảng cáo)
3. Các CTCT
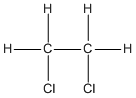 hay
hay 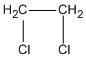
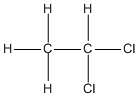 hay
hay 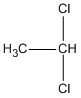
Bài 4.34. Hỗn hợp M chứa hai chất hữu cơ thuộc cùng dãy đồng đẳng và hơn kém nhau 2 nguyên tử cacbon. Nếu làm bay hơi 7,28 g M thì thể tích hơi thu được đúng bằng thể tích của 2,94 g khí N2 ở cùng điều kiện. Để đốt cháy hoàn toàn 5,20 g hỗn hợp M cần dùng vừa hết 5,04 lít 02 (đktc). Sản phẩm cháy chỉ gồm C02 và hơi nước với thể tích bằng nhau.
Hãy xác định công thức phân tử và phần trăm khối lượng từng chất trong hỗn hợp M.
Số mol 2 chất trong 7,28g M: \(\frac{{2,94}}{{28}}\) = 0,105 (mol)
Số mol 2 chất trong 5,2g M: \(\frac{{0,105.5,2}}{{7,28}}\) = 0,075 (mol).
Theo định luật bảo toàn khối lượng:
\({m_{C{O_2}}} + {m_{{H_2}O}} = {m_M} + {m_{{O_2}}} = 5,2 + \frac{{5,04}}{{22,4}}.32 = 12.4(g)\)
Theo đầu bài, số mol \(C{O_2}\) = số mol \({H_2}O\) = n.
44n + 18n = 12,4 \( \Rightarrow \) n = \(\frac{{12,4}}{{62}}\) = 0,2 (mol)
Advertisements (Quảng cáo)
Các chất trong hỗn hợp có chứa C, H và có thể có O. Chất thứ nhất là \({C_{\rm{x}}}{H_y}{O_z}\) (a mol) và chất thứ 2 là \({C_{{\rm{x + 2}}}}{H_{y + 4}}{O_z}\) (b mol).
\(\left\{ \begin{array}{l}
a + b = 0,075(1)\\
(12{\rm{x}} + y + 16{\rm{z}})a + (12{\rm{x}} + y + 16{\rm{z}} + 28)b = 5,2(2)
\end{array} \right.\)
\({C_{\rm{x}}}{H_y}{O_z} + (x + \frac{y}{4} – \frac{z}{2}){O_2} \to xC{O_2} + \frac{y}{2}{H_2}O\)
a mol xa mol \(\frac{{ya}}{2}\) mol
\({C_{{\rm{x + 2}}}}{H_{y + 4}}{O_z} + (x + \frac{y}{4} – \frac{z}{2} + 3){O_2} \to (x + 2)C{O_2} + \frac{{y + 4}}{2}{H_2}O\)
b mol (x+2)b mol \(\frac{{(y + 4)b}}{2}\)
xa + (x + 2)b = 0,2 (3)
\(\frac{{y{\rm{a + }}(y + 4)b}}{2} = 0,2\) (4)
Giải hệ phương trình :
Từ (3) ta có x(a + b) + 2b = 0,200
2b = 0,200 – 0,0750x
b = 0,100 – 0,0375x
0 < b < 0,075 0 < 0,100 – 0,0375x < 0,0750
0,660 < X < 2,66
Trong khoảng này có 2 số nguyên là 1 và 2.
Nếu x= 1. b = 0,100 – 3.75.\({10^{ – 2}}\) = 0,0625
a = 0,0750 – 0,0625 = 0,0125.
Thay giá trị cùa a và b vào (4) ta có :
0125y + 0,0625(y + 4) = 0,400 \( \Rightarrow \) y = 2.
Thay x = 1, y = 2;a = 0,0125, b = 0,0625 vào (2):
(14 + 16z).0,0125 + (42 + 16z).0,0625 = 5,20 \( \Rightarrow \) z = 2.
\(C{H_2}{O_2}\) chiếm : \(\frac{{0,0125.46}}{{5,2}}\). 100% = 11,1%.
C3H602 chiếm : 100% – 11,1% = 88,9%.
Nếu x = 2 . b = 0,100 – 0,0375 X 2 = 0,0250
a = 0,0750 – 0,0250 = 0,05
từ đó tìm tiếp, ta được y = 4 và z = 2.
% khối lượng của C2H402: \(\frac{{0,05.60}}{{5,2}}\). 100% = 57,7%.
% khối lương của \({C_4}{H_8}{O_2}\) : 100% – 57,7% = 42,3%.

