Bài 1: Thế nào là anđehit? Viết công thức cấu tạo của các anđehit có công thức phân tử C4H8O và gọi tên chúng.
Các anđehitt C4H8O: CH3-CH2-CH2-CHO anđehit butyric (butanal).
CH3– CH –CHO anđehit isobutiric (2- metyl propanal).
Bài 2: Viết các phương trình hóa học để chứng tỏ rằng, anđehit vừa có tính oxi hóa vừa có tính khử.
Anđehit bị H2 hoặc LiAlH4 khử thành ancol
R-CH=O + H2 —> R-CH2OH
R-CH=O + LiAlH4 + HCl —> R-CH2OH + AlH3 + LiCl
– Dưới tác dụng của hỗn hống Zn/Hg trong HCl, anđehit bị khử thành hiđrocacbon
R-CH=O + Na-Hg + 4HCl —> R-CH3 + NaCl + HgCl2 + H2O
Như vậy, anđehit còn có tính oxi hóa
Bài 3: Hoàn thành dãy chuyển hóa sau bằng các phương trình hóa hoc:
Advertisements (Quảng cáo)
Metan-> metyl clorua-> methanol-> metanal -> axit fomic
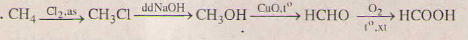
Bài 4: Cho 1,0 ml dung dịch fomanđehit 5 % và 1,0 ml dung dịch NaOH 10,0 % vào ống nghiệm, sau đó thêm tiếp từng giọt dung dịch CuSO4và lắc đều cho đến khi xuất hiện kết tuả. Đun nóng phần dung dịch phía trên, thấy có kết tủa màu đỏ gạch của Cu2O. Giải thích hiện tượng thí nghiệm và viết phương trình hóa học.
Advertisements (Quảng cáo)
CuSO4 + 2NaOH -> Cu(OH)2 + Na2SO4
HCHO + 2Cu(OH)2 + NaOH -> HCOONa + Cu2O + 3H2O
Bài 5: Cho 50,0 gam dung dịch anđehit axetic tác dụng với dung dịch AgNO3 trong NH3 (đủ) thu được 21,6 gam Ag kết tủa. Tính nồng đồ % của anđehit axetic trong dung dịch đã dùng.
Đáp số C% = 8,8%
CH3-CH=O + 2AgNO3 + H2O + 3NH3 -> R-COONH4 + 2NH4NO3 + 2Ag
1 mol 2 mol
0,100 mol 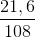 = 0,2 (mol)
= 0,2 (mol)
MCH3CHO = 0,1. 44,0 = 4,4 (g); C%CH3CHO = 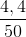 . 100% = 8,8%
. 100% = 8,8%

